Тесты по теме Химические реакции. Часть 5
Предлагаем вашему вниманию тесты по теме Химические реакции с подробными видео-объяснениями (даны сразу после условий задания) и ответами (приведены в конце страницы).
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
1. Фенолфталеин, лакмус и метилоранж по отдельности изменяют свою окраску в водном растворе вещества, которое образуется в результате реакции соединения между веществами, формулы которых:
1) K, HI
2) SO3, H2O
3) Li2O, H2O
4) Na, H2O
2. В системе протекает обратимая гомогенная реакция 3H2 + N2 ↔ 2NH3. На рисунке изображены графики зависимости концентраций реагирующих веществ от времени. Определите выход (%) продукта реакции на момент установления равновесия: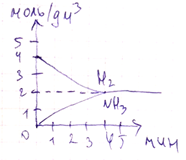
1) 50
2) 66,7
3) 75
4) 100
3. Выберите верные утверждения для равновесной системы, в которой протекает реакция CO(г) + 2H2(г) ↔ CH3OH(г) + Q:
а) при понижении температуры увеличивается как скорость прямой реакции, так и обратной;
б) добавление водорода способствует протеканию прямой реакции;
в) при повышении давления равновесие смещается в сторону исходных веществ;
г) повышение температуры приводит к уменьшению выхода продуктов реакции.
1) б, г
2) б, в
3) а, в
4) б, в, г
4. В системе протекает обратимая гомогенная реакция 2HI (г) ↔ H2 (г) + I2 (г). На рисунке изображены графики зависимости молярных концентраций иодоводорода и иода от времени. Установите практический выход (%) газообразного иода в момент установления химического равновесия: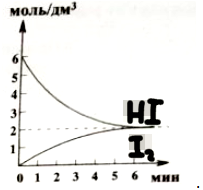
1) 45
2) 59
3) 67
4) 73
5) 85
5. В равновесной системе SO2Cl2 (г) ↔ SO2 (г) + Cl2 (г) – Q на смещение равновесия влево влияют:
а) увеличение давления;
б) уменьшения давления;
в) увеличение температуры;
г) уменьшение температуры;
д) выведение из системы SO2;
е) добавление в систему Cl2.
1) а, в, д
2) а, г, д
3) а, г, е
4) б, в, д
5) б, г, е
6. Сера реагирует с концентрированным раствором гидроксида калия по схеме S + KOH → K2SO3 + K2S + H2O. Укажите массу (г) прореагировавшего исходного вещества, которое не проявляет окислительно-восстановительных свойств, если в результате этой реакции образовалась вода массой 6,48 г:
1) 6,48
2) 11,52
3) 20,16
4) 23,04
5) 40,32
7. В одном и том же направлении смещается равновесие при понижении температуры и повышении давления в системах:
а) SO2 (г) + Cl2 (г) ↔ SO2Cl2 (г) + Q;
б) 2H2 (г) + O2 (г)↔ 2H2O (г) + Q;
в) C3H8 (г) ↔ C3H4 (г) + 2H2 (г) – Q;
г) H2 (г) + Cl2 (г) ↔ 2HCl (г) + Q;
д) 2CO (г) + O2 (г) ↔ 2CO2 (г) + Q;
е) H2 (г) + I2 (к) ↔ 2HI (г) + Q.
1) а, в, д
2) а, г, е
3) б, в, г
4) б, г, е
5) а, б, в, д
8. Выберите правильную последовательность окислительно-восстановительных процессов, которые происходят с кобальтом по схеме превращений
Co → Co3O4 → CoO → Co:
1) окисление, окисление, восстановление
2) окисление, восстановление, окисление
3) восстановление, восстановление, восстановление
4) восстановление, восстановление, окисление
5) восстановление, окисление, восстановление
9. В закрытом сосуде протекает обратимая реакция 2SO2 (г) + O2 (г) ↔ 2SO3 (г) + Q. При повышении температуры:
а) равновесие смещается вправо;
б) скорость прямой реакции увеличивается;
в) скорость прямой реакции уменьшается;
г) скорость обратной реакции увеличивается;
д) скорость обратной реакции уменьшается;
е) равновесие смещается влево.
1) а, б, д
2) а, в, г
3) б, г, е
4) в, г, е
5) в, д, е
10. Оксид железа (III) полностью растворили в необходимом количестве разбавленной серной кислоты. В полученный раствор опустили гранулы цинка. Укажите тип реакции, которая НЕ протекала в описанном эксперименте:
1) замещение
2) обратимая
3) окислительно-восстановительная
4) НЕкаталитическая
5) обмена
11. Верные утверждения для равновесной системы C2H2 (г) + 2Cl2 (г) ↔ C2H2Cl4 (г) + Q:
а) повышение температуры смещает равновесие в сторону исходных веществ;
б) понижение температуры увеличивает скорость прямой реакции;
в) выведение ацетилена из равновесной системы способствует протеканию прямой реакции;
г) повышение давления приводит к смещению равновесия влево;
д) добавление хлора смещает равновесие вправо.
1) а, в, д
2) а, в
3) а, д
4) б, в, г
5) г, д
12. Кислород в лаборатории можно получить по реакции, схема которой KMnO4 + H2O2 + H2SO4 → O2↑ + MnSO4 + K2SO4 + H2O. Укажите массу (г) продукта восстановления, если при н.у. выделился кислород объёмом 0,336 дм3:
1) 0,453
2) 0,522
3) 0,906
4) 2,265
5) 4,53
13. НЕ относят к окислительно-восстановительным реакцию, описанную уравнением:
1) (CuOH)2CO3 = 2CuO + CO2 + H2O
2) Na2SO3 + H2O2 =Na2SO4 + H2O
3) NaH + H2O = NaOH + H2
4) S + O2 = SO2
5) 5K2S + 8KMnO4 + 12H2SO4 = 9K2SO4 + 8MnSO4 + 12H2O
Ответы:
-
3
-
3
-
1
-
3
-
3
-
5
-
5
-
2
-
3
-
2
-
3
-
3
-
1
Также предлагаем вам сборку видео-уроков на эту тему:
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Посмотреть видео-объяснения каждого задания ЦТ, РТ и ДРТ всех лет, а также получить условия всех пробных, тренеровочных и реальных вариантов ЕГЭ, вы можете получив полный доступ к сайту кликнув здесь «Получить все материалы сайта»
А также:
- Просмотреть все тесты по органической химии
- Просмотреть все тесты по неорганической химии
- Посмотреть пробные варианты ЦТ вы можете здесь, нажав на эту строку
- Посмотреть пробные и реальные варианты ЕГЭ вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Больше заданий РТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЦТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЕГЭ вы можете найти здесь, нажав на эту строку
- Все видео-объяснения вы можете найти на YouTube канале, нажав на эту строку
