Предлагаем вашему вниманию десятый пробный вариант РТ по химии 2020/2021 для подготовки к ЦТ по химии 2021, ответы представлены в конце страницы.
Скачать РТ по химии 2020/2021. Пробный вариант 10
ВНИМАНИЕ: все задания составлены автором самостоятельно и не являются копией заданий ЦТ и РТ. Если вам необходимы оригинальные задания, то вам надо записываться на этапы РТ (на сайте РИКЗ) и покупать сборники реальных заданий ЦТ и РТ в книжных магазинах.
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
Вариант 10
Для получения полного доступа к сайту переходите по ссылке: http://www.yoursystemeducation.com/poluchit-video/. В полном доступе вы найдёте условия и видео-объяснения заданий-аналогов из всех этапов РТ начиная с 2014 года, а также всех заданий-аналогов ЦТ начиная с самого первого ЦТ 2004 года.
Вариант содержит 44 задания и состоит из части А (28 заданий) и части В (16 заданий). На выполнение всего теста отводится 150 минут. Необходимые справочные материалы – «Периодическая система химических элементов Д.И. Менделеева», «Растворимость кислот, оснований и солей в воде», Электрохимический ряд активности металлов» — приведены в конце теста.
При расчётах принять молярный объём газа (Vm) 22,4 дм3/моль. Значения относительных атомных масс химических элементов (кроме хлора, для которого Ar = 35,5) следует округлять до целого числа. При решении заданий можно пользоваться микрокалькулятором.
Часть А
Для получения приближённого значения чисел в промежуточных расчётах округлите их до третьего знака после запятой по правилам округления. Конечный результат округлите, ориентируясь на числа, предложенные в ответе.
В каждом задании только ОДИН из предложенных вариантов ответа является верным.
А1. Укажите относительную атомную массу элемента, в состав атома которого входит 8 электронов:
1) 4
2) 8
3) 16
4) 32
5) 48
А2. Элемент s-семейства образует катион Э+ с электронной конфигурацией:
1) 1s2
2) 1s22s22p63s1
3) 1s22s22p63s2
4) 1s22s22p63s23p4
5) 1s22s22p63s23p6
А3. Ряд, в котором элементы расположены в порядке увеличения значения электроотрицательности:
1) фосфор, азот, углерод
2) германий, кремний, алюминий
3) кислород, сера, фосфор
4) селен, бром, хлор
5) водород, литий, натрий
А4. Выберите ряд, в котором указаны вещества с ковалентной полярной связью:
1) ртуть, сера, сероводород
2) фтор, черный фосфор, азот
3) сернистая кислота, вода, хлороводород
4) бром, этан, оксид бария
5) кальций, стронций, барий
А5. Соединение, в котором азот имеет низшую степень окисления:
1) NOCl3
2) NCl3
3) N2
4) HNO3
5) Li3N
А6. Название вещества немолекулярного соединения:
1) иодоводород
2) чёрный фосфор
3) азот
4) белый фосфор
5) ромбическая сера
А7. Имеются порции веществ одинакового объёма (н.у.). Наибольшее число молекул содержит порция:
1) аргона
2) этанола
3) аммиака
4) фтора
5) углекислого газа
А8. Укажите вещества, при взаимодействии которых образуется оксид, не образующий солей:
1) оксид цинка и раствор гидроксида натрия
2) нитрат аммония и гидроксид калия
3) азот и кислород
4) серебро и концентрированная серная кислота
5) сульфид алюминия и вода
А9. Укажите формулы веществ, с которыми при комнатной температуре реагирует раствор гидроксида калия:
1) NaCl, Fe(OH)2, ZnO
2) SO2, HCl, Ag
3) NO2, SiO, Na2O
4) Al, HCl, O2
5) SO3, BeO, CuCl2
А10. Бромоводородную кислоту можно использовать для осуществления превращения в одну стадию:
1) K2SiO3 → H2SiO3
2) Na2SO4 → H2SO4
3) NaNO3 → NaBr
4) Cu → CuBr2
5) FeBr2 → FeBr3
А11. Дана схема превращений: ![]() Вещество Y реагирует с:
Вещество Y реагирует с:
1) NaNO3 и Mg
2) NaNO3 и NaOH
3) Mg и NaOH
4) NaOH и Cu
5) NaNO3 и Cu
А12. Кислород получают термическим разложением:
1) H2SO4
2) Zn(NO3)2
3) Cu(OH)2
4) CaSO3
5) H2O
А13. Азот как ПРОСТОЕ ВЕЩЕСТВО:
1) не проявляет валентности, равной номеру группы
2) влияет на качество и объём урожая
3) в высшей степени окисления является только окислителем
4) реагирует с литием при комнатной температуре
5) входит в состав аммиака
А14. Карбонат кальция в морской ракушке можно обнаружить с помощью (все электролиты представлены в виде водных растворов):
1) Ba(OH)2
2) NaHCO3
3) ZnCl2
4) MgF2
5) HI
А15. Выберите пары металлов, в которых первый НЕ вытесняет второй из растворов солей:
1) K, Cu
2) Cd, Sn
3) Mn, Pb
4) Al, Zn
5) Fe, Ag
А16. Для металлов IIA группы НЕВЕРНОЕ утверждение:
1) имеют постоянную валентность в соединениях
2) гидроксиды при нагревании могут терять более 30% по массе
3) все оксиды (за исключением оксидов магния и бериллия) вступают в реакции соединения с водой при комнатной температуре с образованием щелочей
4) при добавлении их (кроме Be и Mg) в водный раствор фенолфталеина появляется малиновая окраска
5) все, кроме Be и Mg, являются щелочно-земельными металлами
А17. Укажите случай, в котором происходит увеличение массы цинковой пластинки при выдерживании её в разбавленном водном растворе:
1) гидроксида натрия
2) хлорида золота (III)
3) соляной кислоты
4) хлорида меди (II)
5) нитрат железа (III)
А18. При добавлении твёрдого карбоната натрия к избытку раствора пропановой кислоты:
1) водородный показатель уменьшается
2) образуется осадок
3) число пропионат-анионов увеличивается
4) выделяется газ
5) электропроводность раствора уменьшается
А19. Укажите растворимость соли в 100 г воды при 30С, если её массовая доля в насыщенном при этой температуре растворе равна 17,95%:
1) 18
2) 21,9
3) 30,2
4) 117,95
5) 300
А20. Укажите коэффициент перед восстановителем в уравнении химической реакции обжига сульфида цинка в избытке кислорода:
1) 2
2) 3
3) 5
4) 9
5) 11
А21. Модель молекулы пентана изображена на рисунке:
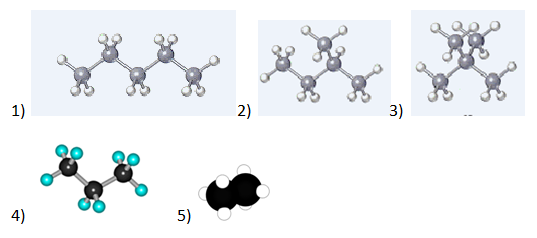 А22. Ацетилен взаимодействует с каждым веществом ряда:
А22. Ацетилен взаимодействует с каждым веществом ряда:
1) He, HBr, H2S
2) Cl2, H2O, NaBr
3) O2, KCl, HBr
4) HCl, Br2, O2
5) F2, C2H4, C
А23. Укажите название вещества, которое не взаимодействует с раствором брома в тетрахлористом углероде:
1) 4-метилгексен-1
2) бензол
3) дивинил
4) пропин
5) стирол
А24. Укажите название конечного вещества, которое образуется в результате превращений ![]() 1) глицерин
1) глицерин
2) пропанол-1
3) ацетон
4) пропаналь
5) акриловая кислота
А25. При комнатной температуре фенол образуется в результате:
1) взаимодействия бензола с водой в присутствии солей двухвалентной ртути
2) взаимодействия циклогексана с твёрдым гидроксидом натрия
3) гидролиза сложного эфира фенола и уксусной кислоты избытком раствора гидроксида натрия
4) ароматизации гексана
5) взаимодействия вещества, формула которого C6H5OK с бромоводородной кислотой
А26. В результате щелочного гидролиза вещества 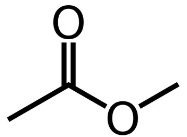 гидроксидом калия, образуется:
гидроксидом калия, образуется:
1) метанол и уксусная кислота
2) метанолят калия и этановая кислота
3) метанолят калия и этаноат калия
4) метанол и муравьиная кислота
5) метанол и ацетат калия
А27. Число гидроксильных групп и альдегидных групп соответственно в молекуле глюкозы, находящейся в линейной форме, равно:
1) 5 и 1
2) 3 и 2
3) 4 и 1
4) 6 и 0
5) 2 и 3
А28. Полимер, строение которого указано на рисунке  , образуется из мономера:
, образуется из мономера:
1) изопрен
2) бутен-1
3) бутен-2
4) пропилен
5) ацетилен
Часть В
При решении задач в промежуточных расчётах для получения приближенного значения чисел округлите их до третьего знака после запятой по правилам округления, а конечный результат – до целого числа. Единицы измерения числовых величин не указывайте.
В1. Установите соответствие между названием органического вещества и функциональной группой, которая входит в состав молекулы соответствующего вещества.
| НАЗВАНИЕ ВЕЩЕСТВА | ФУНКЦИОНАЛЬНАЯ ГРУППА |
| А) ацетальдегид
Б) фенол В) анилин Г) этиленгликоль |
1. –OH
2. –COOH 3. –CHO 4. –NH2 5. –C(O) – |
Ответ запишите в виде сочетания букв и цифр, например: А2Б2В5Г3 (цифры могут повторяться).
В2. Выберите три верных утверждения о бензоле.
- НЕ является гомологом
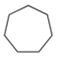
- Длина связи между атомами углерода в бензольном кольце больше, чем между атомами углерода при кратной связи в молекуле пропина.
- При взаимодействии с хлором в присутствии солей трёхвалентного железа образуются хлороводород и хлорбензол.
- При реакции со смесью концентрированных серной и азотной кислот даёт соединение
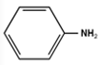
- Количество атомов водорода в молекуле на 1 больше, чем атомов углерода.
- Является гомологом анилина.
В3. Вычислите сумму молярных масс (г/моль) органической соли Х6 и неорганического вещества немолекулярного строения Х7, полученных в результате превращений:
 В4. Вычислите суммарную массу (г) фосфоросодержащих веществ Х и Y, которые получены из двух одинаковых порций оксида фосфора (V) по 35,5 г каждая:
В4. Вычислите суммарную массу (г) фосфоросодержащих веществ Х и Y, которые получены из двух одинаковых порций оксида фосфора (V) по 35,5 г каждая:
 В5. Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами в этой реакции.
В5. Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами в этой реакции.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) Fe + H2SO4 (разб.) →
Б) Fe + H2SO4 (конц.) нагревание → В) Fe + Fe2(SO4)3 (p-p) → Г) Fe(OH)2 + H2SO4 (разб.) → |
1. Fe2(SO4)3 + H2
2. FeSO4 + H2O 3. Fe2(SO4)3 + SO2 + H2O 4. FeSO4 + H2 5. FeSO4 + SO2 6. FeSO4 |
Ответ запишите в виде сочетания букв и цифр, например: А2Б4В5Г3.
В6. Определите сумму молярных масс (г/моль) углеродсодержащего вещества Д и натрийсодержащего вещества Е, если вещество В при н.у. имеет газообразное агрегатное состояние:
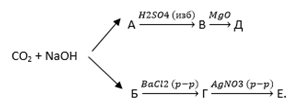 В7. Дана схема превращений, в которой реагенты, необходимые для превращений, зашифрованы буквами.
В7. Дана схема превращений, в которой реагенты, необходимые для превращений, зашифрованы буквами.
![]() Выберите реагенты для осущуествления превращений, представленных выше (соли находятся в виде разбавленных водных растворов):
Выберите реагенты для осущуествления превращений, представленных выше (соли находятся в виде разбавленных водных растворов):
1) SO2;
2) O2;
3) Ba(NO3)2;
4) H2O;
5) S;
6) Ba(OH)2.
Ответ запишите в виде сочетания букв и цифр, например: А1Б2В5Г3.
В8. Установите соответствие между парой веществ и реактивом, с помощью которого можно различить эти вещества.
| А) этиленгликоль (р-р) и аланилаланин (р-р)
Б) муравьиная кислота (р-р) и метанол (р-р) В) толуол и циклопентанол Г) гексан и гексин-1 |
1. CH3COONa
2. Br2 (H2O) 3. Cu(OH)2 4. K 5. FeCl3 |
Ответ запишите в виде сочетания букв и цифр, например: А2Б2В5Г3 (цифры могут повторяться).
В9. Установите соответствие между названием вещество и областью его практического применения.
| А) иод
Б) фенол В) железо Г) кокс |
1. Производство лекарств и пластмасс
2. Выплавка чугуна 3. Антисептик 4. Антиоксидант 5. Катализатор для процессов гидрирования |
Ответ запишите в виде сочетания букв и цифр, например: А2Б2В5Г3 (цифры могут повторяться).
В10. Бесцветный газ А, являющийся самым лёгким на планете, при высокой температуре и давлении, а также в присутствии катализатора реагирует с азотом. При этом образуется бесцветный газ Б с характерным резким запахом. Этот газ очень хорошо растворим в воде и изменяет окраску лакмуса на синюю. Газ Б реагирует с газом В при н.у., который, в свою очередь, получают из хлорида натрия действием концентрированной серной кислоты при нагревании. В результате взаимодействия газов образуется соль Г, которая в реакции с твёрдой каустической содой (вещество Д) снова даёт газ Б. Установите соответствие между зашифрованным веществом и его молярной массой (г/моль).
| А
Б В Г Д
|
1. 40
2. 17 3. 2 4. 53,5 5. 36,5 6. 58,5 |
Ответ запишите в виде сочетания букв и цифр, например: А2Б4В5Г3Д1.
В11. Рассчитайте объём кислорода (дм3, н.у.), который необходим для полного сгорания смеси массой 40,2 г, состоящий из алканов, которые являются ближайшими гомологами. Про эту смесь известно, что относительная плотность её по гелию равна 20,1.
В12. Имеется смесь нитрата аммония и нитрата калия, которая необходима для удобрения территории площадью 10 м2. Рассчитайте массу (г) этой смеси, если известно, что в почву необходимо внести азот массой 4,368 г и калий массой 5,616 г в расчёте на м2.
В13. Продукты стехиометрической реакции между раствором гидроксида стронция и железным купоросом прокипятили до полного завершения всех реакций. В результате получили осадок массой 102,4 г. Рассчитайте массу (г) прореагировавшего кристаллогидрата.
В14. Смесь, состоящую из серы и неизвестного алкана, взятых в мольном отношении 1:5 соответственно, сожгли в избытке кислорода. Образовавшиеся продукты пропустили через избыток гидроксида кальция. В результате образовалась смесь нерастворимых веществ общей массой 157,2 г. Далее с помощью определённых превращений весь сульфит кальция перевели в сульфат. В результате образовалась смесь сульфата и карбоната кальция, которую обработали избытком соляной кислоты, в итоге нерастворимым осталось вещество массой 8,16 г. Укажите сумму всех атомов в одной молекуле неизвестного алкана.
В15. В результате реакции азота с водородом с выходом 70% образовался аммиак. Объёмная доля водорода в полученной газовой смеси стала равной 59%. Рассчитайте объём (дм3) водорода в исходной газовой смеси объёмом 50 дм3 (н.у.).
В16. Зажжённый фосфор, подобно магнию, продолжает гореть в атмосфере углекислого газа. В этом процессе атомы восстановителя отдали 9,03∙1022 электронов. Рассчитайте количесвто теплоты (кДж), которое выделилось в результате этого превращения, если тепловой эффект реакции равен 1014 кДж, а оксид фосфора (V) образуется в виде димера.
Ответы:
Часть А
- 3
- 2
- 4
- 3
- 5
- 2
- 2
- 3
- 5
- 1
- 3
- 2
- 4
- 5
- 1
- 2
- 2
- 4
- 2
- 1
- 1
- 4
- 2
- 3
- 5
- 5
- 1
- 4
Часть В:
- А3Б1В4Г1
- 123
- 225
- 177
- А4Б3В6Г2
- 169
- А2Б4В1Г6
- А3Б3В4Г2
- А3Б1В2Г2
- А3Б2В5Г4Д1
- 100
- 213
- 111
- 17
- 41
- 8
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
Посмотреть видео-объяснения каждого задания ЦТ, РТ и ДРТ всех лет вы можете получив полный доступ к сайту кликнув здесь «Получить все материалы сайта»
- Посмотреть все пробные варианты ЦТ 2021 вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Больше заданий РТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЦТ вы можете найти здесь, нажав на эту строку
- Наш канал на YouTube вы можете посмотреть, нажав на эту строку
