Скорость химической реакции – это изменение концентрации реагирующих веществ в единицу времени.
При гомогенных реакциях пространством реакции обозначается объем реакционного сосуда, а при гетерогенных — поверхность, на которой протекает реакция. Концентрацию реагирующих веществ обычно выражают в моль/л — количестве молей вещества в 1 литре раствора.
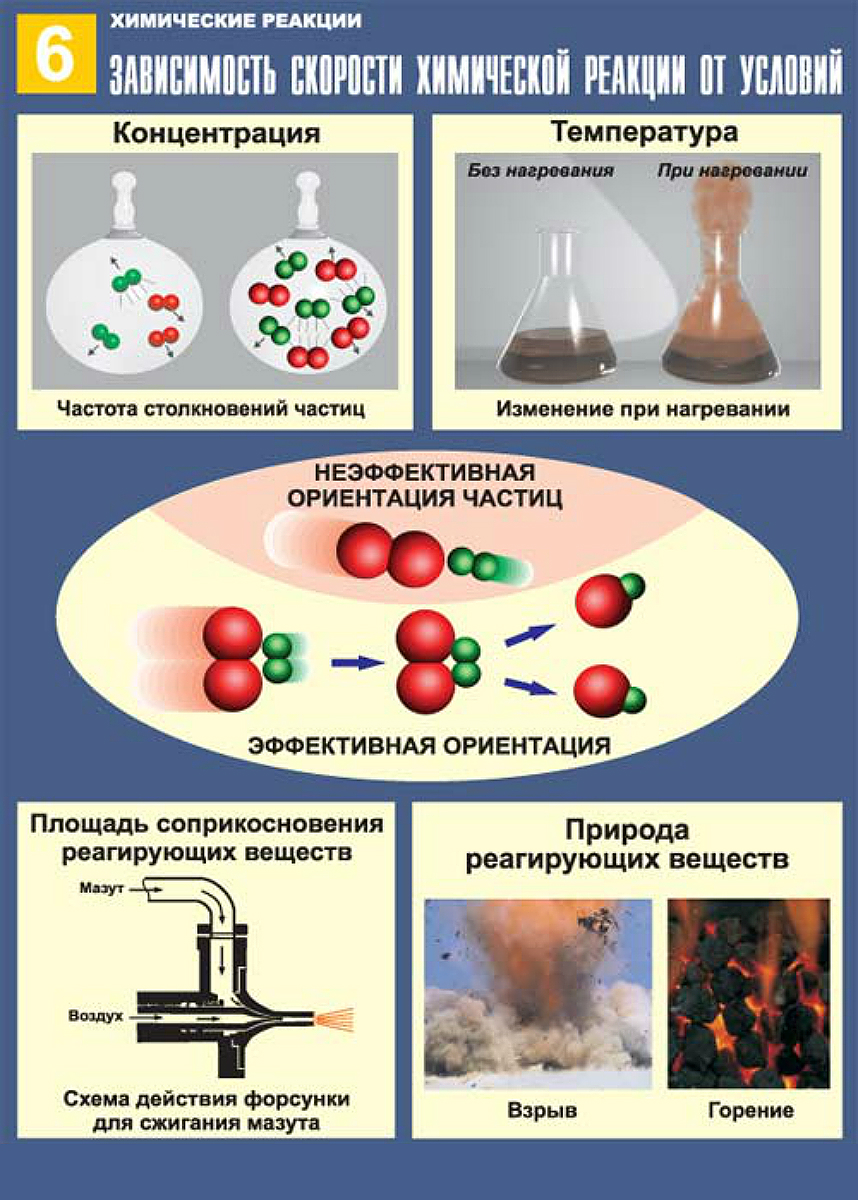
Скорость химической реакции зависит от природы реагирующих веществ, концентрации, температуры, давления, поверхности соприкосновения веществ и ее характера, присутствия катализаторов.
Увеличение концентрации веществ, вступающих в химическое взаимодействие, приводит к увеличению скорости химической реакции. Это происходит потому, что все химические реакции проходят между некоторым количеством реагирующих частицами (атомами, молекулами, ионами). Чем больше этих частичек в объеме реакционного пространства, тем чаще они соударяются и происходит химическое взаимодействие. Химическая реакция может протекать через один или несколько элементарных актов ( соударений). На основании уравнения реакции можно записать выражение зависимости скорости реакции от концентрации реагирующих веществ. Если в элементарном акте участвует лишь одна молекула (при реакции разложения), зависимость будет иметь такой вид:
v = k*[A]
Это уравнение мономолекулярной реакции. Когда в элементарном акте происходит взаимодействие двух разных молекул, зависимость имеет вид:
v = k*[A]*[B]
Реакция называется бимолекулярной. В случае соударения трех молекул справедливо выражение:
v = k*[A]*[B]*[C]
Реакция называется тримолекулярной. Обозначения коэффициентов:
v — скорость реакции;
[А], [В], [С] — концентрации реагирующих веществ;k — коэффициент пропорциональности; называется константой скорости реакции.
Если концентрации реагирующих веществ равны единице ( 1 моль/л) или их произведение равно единице, то v = k.. Константа скорости зависит от природы реагирующих веществ и от температуры. Зависимость скорости простых реакций (т. е. реакций, протекающих через один элементарный акт) от концентрации описывается законом действующих масс: скорость химической реакции прямо пропорциональна произведению концентрации реагирующих веществ, возведенных в степень их стехиометрических коэффициентов.
Для примера разберем реакцию 2NO + O2 = 2NO2.
В ней v = k*[NO]2*[O2]
В случае, когда уравнение химической реакции не соответствует элементарному акту взаимодействия, а отражает лишь связь между массой вступивших в реакцию и образовавшихся веществ, то степени у концентраций не будут равны коэффициентам, стоящим перед формулами соответствующих веществ в уравнении реакции. Для реакции, которая протекает в несколько стадий, скорость реакции определяется скоростью самой медленной ( лимитирующей) стадии.
Такая зависимость скорости реакции от концентрации реагирующих веществ справедлива для газов и реакций, проходящих в растворе. Реакции с участием твердых веществ не подчиняются закону действующих масс, так как взаимодействие молекул происходит лишь на поверхности раздела фаз. Следовательно, скорость гетерогенной реакции зависит еще и от величины и характера поверхности соприкосновения реагирующих фаз. Чем больше поверхность – тем быстрее будет идти реакция.
Влияние температуры на скорость химической реакции
Влияние температуры на скорость химической реакции определяется правилом Вант-Гоффа: при повышении температуры на каждые 10°C скорость реакции увеличивается в 2-4 раза. Математически это правило передается следующим уравнением:
vt2 = vt1* g(t2-t1)/10
где vt1 и vt2 — скорости реакций при температурах t2 и t1; g — температурный коэффициент реакции — число, показывающее, во сколько раз увеличивается скорость реакции при повышении температуры на каждые 10°C. Такая значительная зависимость скорости химической реакции от температуры объясняется тем, что образование новых веществ происходит не при всяком столкновении реагирующих молекул. Взаимодействуют только те молекулы ( активные молекулы), которые обладают достаточной энергией, чтобы разорвать связи в исходных частицах. Поэтому каждая реакция характеризуется энергетическим барьером. Для его преодоления молекуле необходима энергия активации — некоторая избыточная энергия, которой должна обладать молекула для того, чтобы ее столкновение с другой молекулой привело к образованию нового вещества. С ростом температуры число активных молекул быстро увеличивается, что приводит в резкому возрастанию скорости реакции по правилу Вант-Гоффа. Энергия активации для каждой конкретной реакции зависит от природы реагирующих веществ.
Теория активных столкновений позволяет объяснить влияние некоторых факторов на скорость химической реакции. Основные положения этой теории:
- Реакции происходят при столкновении частиц реагентов, которые обладают определённой энергией.
- Чем больше частиц реагентов, чем ближе они друг к другу, тем больше шансов у них столкнуться и прореагировать.
- К реакции приводят лишь эффективные соударения, т.е. такие при которых разрушаются или ослабляются «старые связи» и поэтому могут образоваться «новые». Для этого частицы должны обладать достаточной энергией.
- Минимальный избыток энергии, необходимый для эффективного соударения частиц реагентов, называется энергией активации Еа.
- Активность химических веществ проявляется в низкой энергии активации реакций с их участием. Чем ниже энергия активации, тем выше скорость реакции. Например, в реакциях между катионами и анионами энергия активации очень мала, поэтому такие реакции протекают почти мгновенно
Влияние катализатора
Одно из наиболее эффективных средств воздействия на скорость химических реакций — использование катализаторов. Катализаторы — это вещества, которые изменяют скорость реакции, а сами к концу процесса остаются неизменными по составу и по массе. Иначе говоря, в момент самой реакции катализатор активно участвует в химическом процессе, но к концу реакции реагенты изменяют свой химический состав, превращаясь в продукты, а катализатор выделяется в первоначальном виде. Обычно роль катализатора заключается в увеличении скорости реакции, хотя некоторые катализаторы не ускоряют, а замедляют процесс. Явление ускорения химических реакций благодаря присутствию катализаторов носит название катализа, а замедления — ингибирования.
Некоторые вещества не обладают каталитическим действием, но их добавки резко увеличивают каталитическую способность катализаторов. Такие вещества называются промоторами. Другие вещества (каталитические яды) уменьшают или даже полностью блокируют действие катализаторов, этот процесс называется отравлением катализатора.
Существуют два вида катализа: гомогенный и гетерогенный. При гомогенном катализе реагенты, продукты и катализатор составляют одну фазу (газовую или жидкую). В этом случае отсутствует поверхность раздела между катализатором и реагентами.
Особенность гетерогенного катализа состоит в том, что катализаторы (обычно твердые вещества) находятся в ином фазовом состоянии, чем реагенты и продукты реакции. Реакция развивается обычно на поверхности твердого тела.
При гомогенном катализе происходит образование промежуточных продуктов между катализатором и реагирующим веществом в результате реакции с меньшим значением энергии активации. При гетерогенном катализе увеличение скорости объясняется адсорбцией реагирующих веществ на поверхности катализатора. В результате этого их концентрация увеличивается и скорость реакции растет.
Особым случаем катализа является аутокатализ. Смысл его заключается в том, что химический процесс ускоряется одним из продуктов реакции.
Примеры решения задач на скорость реакции
Также вы можете посмотреть ВИДЕО-уроки на эту тему:
И выполнить задания из ЦТ и ЕГЭ на эту тему вы можете здесь