Предлагаем вашему вниманию первый пробный вариант для подготовки к ЦТ по химии 2019.
Скачать РТ 2018/2019 вариант 1
ВНИМАНИЕ: все задания составлены автором самостоятельно и не являются копией заданий ЦТ и РТ. Если вам необходимы оригинальные задания, то вам надо записываться на этапы РТ (на сайте РИКЗ) и покупать сборники реальных заданий ЦТ и РТ в книжных магазинах.
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
Вариант 1
Вариант содержит 50 заданий и состоит из части А (38 заданий) и части В (12 заданий). На выполнение всего теста отводится 150 минут.
При расчётах принять молярный объём газа (Vm) 22,4 дм3/моль. Значения относительных атомных масс химических элементов (кроме хлора, для которого Ar = 35,5) следует округлять до целого числа. При решении заданий можно пользоваться микрокалькулятором. Будьте внимательны! Желаем успеха!
Часть А
Для получения приближённого значения чисел в промежуточных расчётах округлите их до третьего знака после запятой по правилам округления. Конечный результат округлите, ориентируясь на числа, предложенные в ответе.
В каждом задании только ОДИН из предложенных вариантов ответа является верным. В бланке ответов под номером задания поставьте метку (х) в клеточке, соответствующей номеру выбранного варианта ответа.
А1. Атому аргона в основном состоянии соответствует электронная конфигурация частицы:
1) Ca0 2) K+ 3) Cl+1 4) Sc0
А2. Укажите заряд ядра атома натрия:
1) 0 2) +1 3)+11 4) +23
А3. На 2s-энергетическом подуровне расположены все валентные электроны атома:
1) кремния 2) бериллия 3) натрия 4) магния
А4. Неметаллические свойства наиболее выражены у:
1) серы 2) углерода 3) кислорода 4) фосфора
А5. Вещества с ковалентной полярной связью находятся в ряду:
1) NH3, SF6, H2S 2) KF, HF, CF4 3) CO2, N2, HF 4) SO2, NO2, Cl2
А6. Укажите формулу молекулы, в которой степень окисления элемента равна нулю, а валентность равна единице:
1) O2 2) CaC2 3) Cl2 4) CO
А7. Количество атомов, содержащихся в этане количеством 1 моль, составляет:
1) 6∙1023 2) 8 3) 6∙10-23 4) 4,8∙1024
А8. Кислород собирают способом вытеснения:
1) воздуха, держа сосуд вверх дном 3) воздуха, держа сосуд горизонтально
2) воды, держа сосуд вниз дном 4) воздуха, держа сосуд вниз дном
А9. К амфотерным оксидам относится:
1) CrO3 2) SO3 3) CO2 4) Cr2O3
А10. При нагревании гидроксида меди (II) образуются вода и:
1) Сu 2) СuО 3) Сu2О 4) СuОН
А11. Разбавленная серная кислота может реагировать с каждым из двух веществ:
1) серой и магнием 3) оксидом железа (II) и оксидом кремния (IV)
2) гидроксидом калия и хлоридом калия 4) нитратом бария и гидроксидом меди (II)
А12. Выберите верные утверждения о соли, формула которой Na2HPO4:
а) имеет немолекулярное строение;
б) можно получить добавлением NaOH к водному раствору Na3PO4;
в) реагирует с раствором фосфорной кислоты;
г) формульная единица состоит из восьми атомов.
1) а, б 2) а, в, г 3) б, в, г 4) б, в
А13. Установите соответствие между веществом и типом его кристаллической решетки.
| ВЕЩЕСТВО | ТИП КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ |
| 1) поваренная соль
2) серебро 3) углекислый газ 4) графит 5) глюкоза |
а) молекулярная
б) ионная в) атомная г) металлическая |
1) 1б, 2в, 3а, 4а, 5в 2) 1а, 2г, 3а, 4б, 5в
3) 1б, 2г, 3а, 4в, 5а 4) 1в, 2б, 3в, 4г, 5а
А14. Соляная кислота взаимодействует при обычных условиях со всеми веществами набора:
1) КНСО3, Ва, Fe(OH)2 3) СО, Сu, Pb(NO3)2 (р-р)
2) ZnO, KNO3 (р-р), Fe 4) СО2, AgNO3(р-р), Mg
А15. Диоксид серы в промышленности можно получить:
а) обжигом сульфидных руд на воздухе;
б) обработкой сульфитов серной кислотой;
в) действием на сульфатные руды смесью непредельных углеводородов; г) сжиганием серы на воздухе;
д) сжиганием Н2S при недостатке О2;
1) а, б, г 2) а, в, г 3) б, в, д 4) б, г, д
А16. Алюминий обработали очень разбавленной азотной кислотой, прозрачный раствор выпарили досуха, сухой остаток нагрели. В результате образовались газы:
1) NO2, O2, N2O 2) N2O, NO, N2
3) NO2, NO, О2 4) NO, N2, О2
А17. Из 1 кг известняка, не содержащего примесей, получено 0,435 кг негашеной извести. Рассчитайте выход (%) продукта реакции.
1) 43,5 2) 54,6 3) 77,7 4) 87,0
А18. Укажите как изменится масса цинковой пластинки через некоторое время, после того как ее опустили в раствор хлорида железа (II):
1) не изменится 2) увеличится
3) уменьшится 4) пластинка растворится
А19. Массовая доля кислорода в оксиде двухвалентного металла равна 20%. Для металла верными являются утверждения:
а) относится к переходным металлам;
б) оксид реагирует с соляной кислотой;
в) оксид реагирует с водой с образованием основания;
г) в реакции с концентрированной серной кислотой выступает в роли окислителя.
1) а, б, в 2) а, б 3) б, в 4) в, г
2, (изб,конц.р−р)
А20. Дана схема превращений ![]() Известно, что при окислении 1 моль цинка бромом выделяется 894 кДж теплоты. При получении вещества А выделилась теплота количеством 357,6 кДж. Укажите массу (г) цинкосодержащего вещества Б, образовавшегося в результате этих превращений:
Известно, что при окислении 1 моль цинка бромом выделяется 894 кДж теплоты. При получении вещества А выделилась теплота количеством 357,6 кДж. Укажите массу (г) цинкосодержащего вещества Б, образовавшегося в результате этих превращений:
1) 39,6 2) 48 3) 84,4 4) 96
А21. Степень диссоциации (%) азотистой кислоты в растворе, содержащем 0,3 моль ионов NO2— и 1 моль молекул кислоты, составляет:
1) 23 2) 30 3) 41 4) 56
А22. Реакция, равновесие которой сместится влево как при понижении температуры, так и при повышении давления:
1) 2SO3 ⇄ O2 +2SO2 – Q 3) 2CO + O2 ⇄ 2CO2 + Q
2) N2 +O2 ⇄ 2NO – Q 4) 4HCl + O2 ⇄ 2Cl2 + 2H2O + Q
А23. Одновременно не могут находиться в растворе все ионы ряда:
1) Fe3+ К+, Cl—, SO42- 3) Са2+, Li+, NO3—, S2-
2) Fe3+, Na+, NО3—, SO42- 4) Ba2+, Cu2+, ОН—, F—
А24. Массовая доля сульфата калия в насыщенном при 70С растворе равна 24%. Укажите растворимость этой соли (г) в 100 г воды при данной температуре:
1) 24 2) 32 3) 68 4) 76
А25. Лампочка прибора для определения электропроводности станет гореть ярче, если в разбавленный водный раствор гидроксида бария:
1) пропустить углекислый газ 3) капнуть серную кислоту
2) добавить стронций 4) добавить сульфид меди (II)
А26. Высокотемпературная переработка нефтепродуктов, которая приводит к образованию углеводородов меньшей молекулярной массы, имеет название:
1) ароматизация 2) крекинг 3) риформинг 4) изомеризация
А27. Укажите класс углеводородов, к которому относится вещество, представленное на рисунке  :
:
1) алканы 2) алкены 3) алкадиены 4) алкины
А28. Укажите названия аренов, которые изомерны друг другу:
а) орто-ксилол; б) этилбензол; в) метилбензол;
г) 1-метил-3-этилбензол; д) мета-ксилол; е) изопропилбензол
1) а, б, д 2) а, г, е 3) б, в, г 4) а, в, е
А29. Гомологами являются:
1) метанол и фенол 3) бутин-2 и бутен-2
2) глицерин и этиленгликоль 4) 2-метилпропан и 2-метилпентан
А30. Какова гибридизация атомов углерода в следующей молекуле 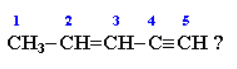 :
:
1)1 – sp3, 2 – sp2, 3 – sp2, 4 – sp, 5 – sp 2) 1 – sp, 2 – sp2, 3 – sp2, 4 – sp, 5 – sp3
3)1 – sp3, 2 – sp, 3 – sp, 4 – sp2, 5 – sp2 4) 1 – sp2, 2 – sp3, 3 – sp3, 4 – sp, 5 – sp
А31. К реакциям замещения относится взаимодействие:
1) этена и воды 2) брома и водорода
3) брома и пропана 4) метана и кислорода
А32. Установите соответствие между названием вещества и его температурой кипения:
| Название вещества | Температура кипения |
| 1. Этанол
2. Бутановая кислота 3. Этан 4. Бутанол-1 |
а) 78,4
б) -88,6 в) 117,4 г) 163 |
1) 1г, 2б, 3в, 4а 3) 1а, 2г, 3в, 4б
2) 1а, 2г, 3б, 4в 4) 1б, 2а, 3г, 4в
А33. Вещество Х может реагировать с фенолом, но не реагирует с этанолом. Это вещество:
1) Na 2) O2 3) HNO3 4) бромная вода
А34. Альдегид может образоваться в результате взаимодействия:
а) ацетилена с подкисленным раствором перманганата калия;
б) уксусной кислоты с избытком кислорода;
в) дихлорэтана с водным раствором щелочи;
г) этилена с кислородом в присутствии хлорида палладия; д) метанола с кислородом в присутствии меди;
е) уксусной кислоты с щелочью;
1) а, в, е 2) б, г, д 3) в, г, д 4) г, д, е
А35. Заполните пропуски соответственно – Водный раствор этановой кислоты имеет … среду, значение рН …, изменяет окраску лакмуса на … .
1) щелочную, больше 7, синюю 3) кислую, меньше 7, красную
2) нейтральную, 7, фиолетовую 4) кислую, больше 7, синюю
А36. В отличие от сахарозы, глюкоза:
а) реагирует с кислородом;
б) реагирует с серной кислотой (конц.);
в) восстанавливается водородом;
г) окисляется аммиачным раствором оксида серебра;
д) реагирует с уксусной кислотой;
е) окисляется гидроксидом меди (II);
1) а, д, е 2) б, в, д 3) б, г, е 4) в, г, е
А37. Сумма коэффициентов в уравнении полного сгорания диэтиламина равна:
1) 31 2) 38 3) 71 4) 75
А38. Реакции полимеризации характерны для:
1) стирола, пропена, этилена 3) пропилена, метаналя, этана
2) стирола, этина, метановой кислоты 4) пропена, бутадиена, гексана
Часть В
При решении задач в промежуточных расчётах для получения приближенного значения чисел округлите их до третьего знака после запятой по правилам округления, а конечный результат – до целого числа.
Единицы измерения числовых величин не указывайте.
Ответы, полученные при выполнении заданий, запишите в бланк ответов. Каждую букву, цифру пишите в отдельной клеточке (начиная с первой) по образцам, указанным в бланке.
В1. Серебристо-белое легкое простое вещество А, обладающее хорошей тепло- и электропроводностью и используемое в авиастроении, реагирует с водой при нагревании, при этом образуются два вещества — простое Б и сложное В. Вещество В реагирует с сильной неорганической кислотой Г, образуя соль, раствор которой при добавлении хлорида бария дает белый осадок, не растворимый в кислотах и щелочах. Найти сумму молярных масс (г/моль) всех зашифрованных веществ, учитывая, что вещество А образовано химическим элементом, который является третим по распространённости в земной коре.
В2. Выберите утверждения, характеризующие фенол.
| 1 | все атомы углерода находятся в состоянии sp3-гибридизации |
| 2 | не реагирует с бромной водой |
| 3 | при н.у. – твердое вещество с запахом, часто розового цвета |
| 4 | между его молекулами образуются водородные связи |
| 5 | проявляет более слабые кислотные свойства, чем этанол |
| 6 | реагирует с азотной кислотой |
Ответ запишите в виде последовательности цифр в порядке возрастания, например: 156.
В3. Определите молярную массу (г/моль) ацетиленового углеводорода, если молярная масса продукта его реакции с избытком бромоводорода в 4 раза больше, чем молярная масса исходного углеводорода.
В4. К 4 см3 смеси метана и ацетилена добавили 8 дм3 водорода. После окончания реакции объём полученной газовой смеси в тех же условиях составил 8 дм3. Определите объёмную долю (%) метана в первоначальной смеси.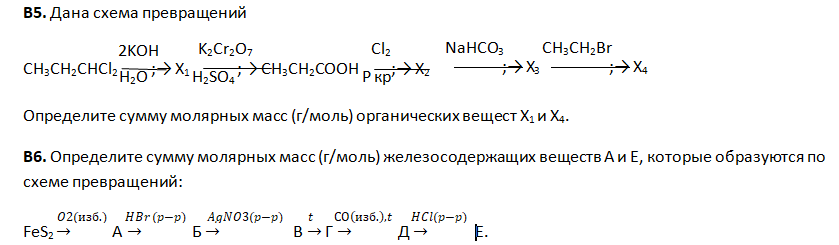 В7. В четырёх пронумерованных пробирках находятся водные растворы неорганических веществ, содержащих ионы Ba2+, NH4+, Br—, H+. О растворах известно следующее:
В7. В четырёх пронумерованных пробирках находятся водные растворы неорганических веществ, содержащих ионы Ba2+, NH4+, Br—, H+. О растворах известно следующее:
- при добавлении к содержимому пробирок 1 и 2 раствора карбоната калия в пробирке 2 образуется осадок белого цвета, а в пробирке 1 выделяется газ, который тяжелее воздуха,
- при добавлении к содержимому пробирок 3 и 4 раствора гидроксида калия из пробирки 4 выделяется газ с характерным запахом, а в пробирке 3 никаких изменений не наблюдается.
| Ионы | Номер пробирки |
| А) Ba2+
Б) NH4+ В) Br— Г) H+ |
1
2 3 4 |
Ответ запишите в виде сочетания букв и цифр, например А3Б1В2Г4.
В8. Для получения вещества по схеме превращений CuCl2 → Cu →CuBr2 →CuCl2 → Cu(OH)2 выберите реагенты или условия протекания реакции из предложенных:
- FeCl2 (p-p); 2. HBr (p-p); 3. Fe;
- 4. KOH (p-p); 5. Br2; 6. t; 7. H2O; 8. Cl2.
Ответ запишите цифрами в порядке следования превращений, например 1254
В9. Смесь нитрата натрия и нитрата металла (III), стоящего до меди в ряду активности, прокалили до постоянной массы, получили газ объёмом 20,16 дм3 (н.у.) и твёрдый остаток массой 40,7 г. После обработки твёрдого остатка водой его масса уменьшилась на 62,654%. Укажите молярную массу (г/моль) неизвестного металла.
В10. Рассчитайте объём (см3) 12%-ного раствора (плотность 0,96 г/см3) аммиака, который можно приготовить из 400 см3 30%-ного (плотность 0,9 г/см3) его раствора.
В11. В твёрдом остатке, полученном при частичном разложении перманганата калия, на два атома марганца приходится семь атомов кислорода. Вычислите массовую долю (%) перманганата калия в этом остатке.
В12. При нагревании аммиака 25% его первоначального объёма распалось на простые вещества. Найдите объёмную долю (%) аммиака в конечной смеси.
Ответы:
Часть А
- 2
- 3
- 2
- 3
- 1
- 3
- 4
- 4
- 4
- 2
- 4
- 2
- 3
- 1
- 1
- 1
- 3
- 3
- 2
- 3
- 1
- 1
- 4
- 2
- 2
- 2
- 4
- 1
- 4
- 1
- 3
- 2
- 4
- 3
- 3
- 4
- 3
- 1
В часть
- 205
- 346
- 54
- 50
- 195
- 287
- А2Б4В3Г1
- 3584
- 56
- 938
- 53
- 60
Если вы заметили ошибку в условии или ответах, то просьба сообщить об этом Александру Конькову в контакт https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Посмотреть видео-объяснения каждого задания ЦТ, РТ и ДРТ всех лет вы можете получив полный доступ к сайту кликнув здесь «Получить все материалы сайта»
- Посмотреть все пробные варианты ЦТ 2019 вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Больше заданий РТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЦТ вы можете найти здесь, нажав на эту строку
- Наш канал на YouTube вы можете посмотреть, нажав на эту строку
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)

в 20 неполное условие
Прошу извинения, исправил.