Представляем вашему вниманию задания (30-35) из реального ЕГЭ 2019 (основная волна, 31 мая 2019 года) с подробными видео-объяснениями,текстовыми решениями и ответами.
Задание 30
Из предложенного перечня веществ выберите вещества, между которыми может протекать окислительно-восстановительная реакция. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций. Составьте электронный баланс, укажите окислитель и восстановитель в этой реакции. Дан следующий перечень веществ (смотри ниже).
Задание 31
Из предложенного перечня веществ выберите вещества, между которыми может протекать реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения только одной из возможных реакций. Дан следующий перечень веществ (смотри ниже).
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 1.
Азотная кислота, сульфат меди(II), ацетат магния, фосфин, хлороводород.
Развернуть/свернуть решение
PH3 + 8HNO3 = H3PO4 + 8NO2 + 4H2O
P-3 – 8e = P+5 8 восстановитель
N+5 + 1e = N+4 1 окислитель
(CH3COO)2Mg + 2HCl = MgCl2 + 2CH3COOH
2CH3COO— + Mg2+ + 2H+ + 2Cl— = Mg2+ + 2Cl— + 2CH3COOH
CH3COO— + H+ = CH3COOH
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 2.
Сульфид серебра(I), азотная кислота, сульфат аммония, нитрат железа(III), ацетат стронция.
Развернуть/свернуть решениеAg2S + 10HNO3 = 2AgNO3 + H2SO4 + 8NO2 + 4H2O (реакция протекает в горячей концентрированной кислоте)
S-2 – 8e = S+6 1 восстановитель
N+5 + 1e = N+4 8 окислитель
Возможны и другие варианты этой же реакции.
(NH4)2SO4 + (CH3COO)2Sr = SrSO4↓ + 2CH3COONH4
2NH4+ + SO42- + 2CH3COO— + Sr2+ = SrSO4↓ + 2CH3COO— + 2NH4+
Sr2+ + SO42- = SrSO4↓
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 3.
Ацетат аммония, нитрат цинка, фосфин, оксид серы(IV), серная кислота.
Развернуть/свернуть решениеPH3 + 4H2SO4 = H3PO4 + 4SO2 + 4H2O
P-3 – 8e = P+5 1 восстановитель
S+6 + 2e = S+4 4 окислитель
2CH3COONH4 + H2SO4 = (NH4)2SO4 + 2CH3COOH
2CH3COO— + 2NH4+ + 2H+ + SO42- = 2NH4+ + SO42- + 2CH3COOH
CH3COO— + H+ = CH3COOH
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 4.
Хлорат калия, гидроксид калия, оксид хрома(III), ацетат меди(II), оксид меди(II).
Развернуть/свернуть решениеCr2O3 + KClO3 + 4KOH = 2K2CrO4 + KCl + 2H2O
2Cr+3 – 6e = 2Cr+6 1 восстановитель
Cl+5 + 6e = Cl-1 1 окислитель
2KOH + (CH3COO)2Cu = Cu(OH)2↓ + 2CH3COOK
2K+ + 2OH— + 2CH3COO— + Cu2+ = Cu(OH)2↓ + 2CH3COO— + 2K+
Cu2+ + 2OH— = Cu(OH)2↓
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 5.
Гипохлорит калия, оксид хрома(III), гидроксид калия, сульфат железа(III), оксид магния.
Развернуть/свернуть решениеCr2O3 + 3KClO + 4KOH = 2K2CrO4 + 3KCl + 2H2O
2Cr+3 – 6e = 2Cr+6 1 восстановитель
Cl+1 + 2e = Cl-1 3 окислитель
6KOH + Fe2(SO4)3 = 2Fe(OH)3↓ + 3K2SO4
6K+ + 6OH— + 2Fe3+ + 3SO42- = 2Fe(OH)3↓ + 6K+ + 3SO42-
Fe3+ + 3OH— = Fe(OH)3↓
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 6.
Сульфат железа(II), оксид марганца(IV), серная кислота, ацетат магния, нитрит аммония.
Развернуть/свернуть решение2FeSO4 + MnO2 + 2H2SO4 = MnSO4 + Fe2(SO4)3 + 2H2O
2Fe+2 — 2e = 2Fe+3 1 восстановитель
Mn+4 + 2e = Mn+2 1 окислитель
Второй вариант NH4NO2 + MnO2 + H2SO4 = MnSO4 + NH4NO3+H2O
N+3 – 2e = N+5 1 восстановитель
Mn+4 + 2e = Mn+2 1 окислитель
(CH3COO)2Mg + H2SO4 = MgSO4 + 2CH3COOH
2CH3COO— + Mg2+ + 2H+ + SO42- = Mg2+ + SO42- + 2CH3COOH
CH3COO— + H+ = CH3COOH
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 7.
Перманганат натрия, сульфид натрия, ацетат стронция, нитрат лития, гидрокарбонат натрия.
Развернуть/свернуть решение2NaMnO4 + 3Na2S + 4H2O = 2MnO2 + 3S + 8NaOH
Mn+7 + 3e = Mn+4 2 окислитель
S-2 – 2e = S0 3 восстановитель
Na2S + (CH3COO)2Sr = SrS↓ + 2CH3COONa
2Na+ + S2- + 2CH3COO— + Sr2+ = SrS↓ + 2CH3COO— + 2Na+
Sr2+ + S2- = SrS↓
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 8.
Перманганат калия, иодид калия, фторид серебра, ацетат магния, нитрат аммония.
Развернуть/свернуть решение2KMnO4 + 6KI + 4H2O = 2MnO2 + 3I2 + 8KOH
Mn+7 + 3e = Mn+4 2 окислитель
2I— – 2e = I20 3 восстановитель
2AgF + (CH3COO)2Mg = MgF2↓ + 2CH3COOAg
2Ag+ + 2F— + 2CH3COO— + Mg2+ = MgF2↓ + 2CH3COO— + 2Ag+
Mg2+ + 2F— = MgF2↓
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 9.
Пероксид водорода, серная кислота, перманганат калия, нитрат аммония, ацетат меди(II).
Развернуть/свернуть решение5H2O2 + 2KMnO4 + 3H2SO4 = 5O2 + 2MnSO4 + K2SO4 + 8H2O
2O-1 – 2e = O20 5 восстановитель
Mn+7 + 5e = Mn+2 2 окислитель
(CH3COO)2Cu + H2SO4 = CuSO4 + 2CH3COOH
2CH3COO— + Cu2+ + 2H+ + SO42- = Cu2+ + SO42- + 2CH3COOH
CH3COO— + H+ = CH3COOH
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 10.
Гипохлорит калия, гидроксид калия, ацетат аммония, хлорид хрома(III), оксид серебра(I).
Развернуть/свернуть решение2CrCl3 + 3KClO + 10KOH = 2K2CrO4 + 9KCl + 5H2O
Cr+3 – 3e = Cr+6 2 восстановитель
Cl+1 + 2e = Cl-1 3 окислитель
KOH + CH3COONH4 = NH3↑ + H2O + CH3COOK
K+ + OH— + CH3COO— + NH4+ = NH3↑ + H2O + CH3COO— + K+
NH4+ + OH— = NH3↑ + H2O
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 11.
Хлорат натрия, гидроксид натрия, ацетат магния, гидроксид хрома(III), гидроксид меди(II).
Развернуть/свернуть решение2Cr(OH)3 + NaClO3 + 4NaOH = 2Na2CrO4+NaCl+5H2O
Cr+3 – 3e = Cr+6 2 восстановитель
Cl+5 + 6e = Cl-1 1 окислитель
2NaOH + (CH3COO)2Mg = Mg(OH)2↓ + 2CH3COONa
2Na+ + 2OH— + 2CH3COO— + Mg2+ = Mg(OH)2↓ + 2CH3COO— + 2Na+
Mg2+ + 2OH— = Mg(OH)2↓
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 12.
Карбонат магния, бром, гидроксид калия, нитрит калия, гидрофосфат калия.
Развернуть/свернуть решение3Br2 + 6KOH → KBrO3 + 5KBr + 3H2O (при нагревании)
Br0 + 1e = Br-1 5 окислитель
Br0 – 5e = Br+5 1 восстановитель
Возможен другой вариант
2KOH + Br2 → KBr + KBrO + H2O
Br0 + 1e = Br-1 1 окислитель
Br0 – 1e = Br+1 1 восстановитель
Возможен другой вариант
KNO2 + Br2 + 2KOH = 2KBr + KNO3 + H2O
N+3 – 2e = N+5 1 восстановитель
Br20 + 2e = 2Br-1 1 окислитель
KOH + K2HPO4 = K3PO4 + H2O
K+ + OH— + 2K+ + HPO42- = 3K+ + PO43- + H2O
OH— + HPO42- = PO43- + H2O
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 13.
Перманганат калия, фосфин, серная кислота, нитрат лития, гидроксид железа(III).
Развернуть/свернуть решение8KMnO4 + 5PH3 + 12H2SO4 → 5H3PO4 + 8MnSO4 + 4K2SO4 + 12H2O
Mn+7 + 5e = Mn+2 8 окислитель
P-3 – 8e = P+5 5 восстановитель
3H2SO4 + 2Fe(OH)3 = Fe2(SO4)3 + 6H2O
6H+ + 3SO42- + 2Fe(OH)3 = 2Fe3+ + 3SO42- + 6H2O
3H+ + Fe(OH)3 = Fe3+ + 3H2O
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 14.
Гидроксид железа(II), гидроксид натрия, хлор, гидрофосфат натрия, карбонат меди(II).
Развернуть/свернуть решение3Cl2 + 6NaOH → NaClO3 + 5NaCl + 3H2O (при нагревании)
Cl0 + 1e = Cl-1 5 окислитель
Cl0 – 5e = Cl+5 1 восстановитель
Возможен другой вариант
2NaOH + Cl2 → NaCl + NaClO + H2O
Cl0 + 1e = Cl-1 1 окислитель
Cl0 – 1e = Cl+1 1 восстановитель
Возможен другой вариант
2Fe(OH)2 + Cl2 + 2NaOH = 2Fe(OH)3 + 2NaCl
Fe+2 – 1e = Fe+3 2 восстановитель
Cl20 + 2e = 2Cl-1 1 окислитель
NaOH + Na2HPO4 = Na3PO4 + H2O
Na+ + OH— + 2Na+ + HPO42- = 3Na+ + PO43- + H2O
OH— + HPO42- = PO43- + H2O
Реальный ЕГЭ 2019. Задание 30 и 31. Вариант 15.
Перманганат калия, сульфид калия, ацетат магния, фосфат калия, гидроксид алюминия.
Развернуть/свернуть решение2KMnO4 + 3K2S + 4H2O = 2MnO2 + 3S + 8KOH
Mn+7 + 3e = Mn+4 2 окислитель
S-2 – 2e = S0 3 восстановитель
3(CH3COO)2Mg + 2K3PO4 = Mg3(PO4)2↓ + 6CH3COOK
6CH3COO— + 3Mg2+ + 6K+ + 2PO43- = Mg3(PO4)2↓ + 6CH3COO— + 6K+
3Mg2+ + 2PO43- = Mg3(PO4)2↓
Задание 32
Реальный ЕГЭ 2019. Задание 32. Вариант 1.
Пероксид натрия обработали оксидом углерода(IV). Выделившийся бесцветный газ прореагировал с раскалённым железом с образованием железной окалины. Полученное вещество растворили в концентрированной азотной кислоте, при этом наблюдали выделение бурого газа. Образовавшуюся соль выделили и добавили к раствору карбоната калия, наблюдали образование бурого осадка и выделение газа. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 2Na2O2 + 2CO2 → 2Na2CO3 + O2↑
- 3Fe + 2O2 → Fe3O4
- Fe3O4 + 10HNO3 → 3Fe(NO3)3 + NO2↑ + 5H2O
- 2Fe(NO3)3 + 3K2CO3 + 3H2O → 2Fe(OH)3↓ + 3CO2↑ + 6KNO3
Реальный ЕГЭ 2019. Задание 32. Вариант 2.
Газ, полученный при нагревании смеси хлорида аммония и гашёной извести, пропустили над нагретым оксидом меди(II). Полученное твёрдое вещество растворили в разбавленной азотной кислоте. Образовавшийся раствор соли подвергли электролизу. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3↑ + 2H2O
- 2NH3 + 3CuO → 3Cu + 3H2O + N2↑
- 3Cu + 8HNO3(разб.) → 3Cu(NO3)2 + 2NO↑ + 4H2O
- 2Cu(NO3)2 + 2H2O → 2Cu↓ + O2↑ + 4HNO3 (электролиз раствора)
Реальный ЕГЭ 2019. Задание 32. Вариант 3.
Смешали растворы сульфата железа(III) и нитрата бария. Выпавший осадок отделили, из оставшегося раствора выделили соль, затем её высушили и прокалили. Твёрдый остаток обработали иодоводородной кислотой. Полученное простое вещество при нагревании вступило в реакцию с концентрированным раствором гидроксида натрия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- Fe2(SO4)3 + 3Ba(NO3)2 → 3BaSO4↓ + 2Fe(NO3)3
- 4Fe(NO3)3 → 2Fe2O3 + 12NO2↑ + 3O2↑
- Fe2O3 + 6HI → 2FeI2 + I2↓ + 3H2O
- 3I2 + 6NaOH(р−р) → NaIO3 + 5NaI + 3H2O (при нагревании)
Реальный ЕГЭ 2019. Задание 32. Вариант 4.
Сульфат меди(II) прореагировал с алюминием. Полученную соль выделили, растворили в воде и добавили к раствору карбоната натрия. Образовавшийся осадок обработали раствором гидроксида натрия. К раствору полученного вещества добавили избыток раствора серной кислоты. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 3CuSO4 + 2Al → Al2(SO4)3 + 3Cu↓
- Al2(SO4)3 + 3Na2CO3 + 3H2O → 2Al(OH)3↓ + 3CO2↑ + 3Na2SO4
- Al(OH)3 + NaOH → Na[Al(OH)4]
- 2Na[Al(OH)4] + 4H2SO4 → Na2SO4 + Al2(SO4)3 + 8H2O
Реальный ЕГЭ 2019. Задание 32. Вариант 5.
Смесь оксида азота(IV) и кислорода поглотили водой, при этом образовалась кислота. Оксид железа(III) сплавили с твёрдым карбонатом натрия, при этом образовался твердый остаток. Этот остаток растворили в избытке раствора полученной кислоты. Образовавшуюся соль железа выделили и поместили в раствор карбоната калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 4NO2 + O2 + 2H2O → 4HNO3
- Fe2O3 + Na2CO3 (тв.) → 2NaFeO2 + CO2↑ (сплавление)
- NaFeO2 + 4HNO3(изб.) → NaNO3 + Fe(NO3)3 + 2H2O
- 2Fe(NO3)3 + 3K2CO3 + 3H2O → 2Fe(OH)3↓ + 3CO2↑ + 6KNO3
Реальный ЕГЭ 2019. Задание 32. Вариант 6.
К раствору серной кислоты добавили оксид меди(II). Через образовавшийся раствор пропустили газ с неприятным запахом, полученный в результате взаимодействия раствора хлорида алюминия с раствором сульфида натрия. Выпавший после пропускания газа черный осадок отделили и обработали концентрированным раствором азотной кислоты. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- CuO + H2SO4 → CuSO4 + H2O
- 2AlCl3 + 3Na2S + 6H2O → 2Al(OH)3↓ + 3H2S↑ + 6NaCl
- CuSO4 + H2S → CuS↓ + H2SO4
- CuS + 8HNO3(конц.) → CuSO4 + 8NO2↑ + 4H2O
Реальный ЕГЭ 2019. Задание 32. Вариант 7.
Смешали растворы бромида железа(II) и гидроксида калия. Выпавший осадок отделили, из оставшегося раствора выделили соль, затем её высушили и обработали концентрированной серной кислотой. Полученное простое вещество разделили на две части. Одну часть поместили в раствор гидроксида калия и нагрели. Вторую часть поместили в раствор, содержащий сульфит калия и гидроксид натрия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- FeBr2 + 2KOH → Fe(OH)2↓ + 2KBr
- 2KBr(тв) + 2H2SO4(конц.) → K2SO4 + Br2 + SO2↑ + 2H2O
- 3Br2 + 6KOH → 5KBr + KBrO3 + 3H2O (при нагревании)
- Br2 + K2SO3 + 2NaOH → 2NaBr + K2SO4 + H2O
Реальный ЕГЭ 2019. Задание 32. Вариант 8.
Фосфат кальция прокалили с оксидом кремния и углём. Образовавшееся простое вещество прореагировало с избытком хлора. Полученный продукт внесли в избыток раствора гидроксида калия. На образовавшийся раствор подействовали раствором гидроксида лития. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- Ca3(PO4)2 + 5C + 3SiO2 → 2P + 5CO + 3CaSiO3
- 2P + 5Cl2 (изб.) → 2PCl5
- 8KOH + PCl5 → K3PO4 + 5KCl + 4H2O
- K3PO4 + 3LiOH → Li3PO4↓ + 3KOH
Реальный ЕГЭ 2019. Задание 32. Вариант 9.
Гидрокарбонат натрия прокалили. Образовавшийся при этом газ (избыток) пропустили через раствор гидроксида калия. К полученному раствору прилили раствор сульфата хрома(III), при этом наблюдали выпадение осадка и выделение бесцветного газа. Осадок отделили и обработали при нагревании раствором, содержащим пероксид водорода и гидроксид натрия, при этом раствор приобрёл жёлтую окраску. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 2NaHCO3 → Na2CO3 + CO2↑ + H2O (прокаливание)
- CO2 + KOH → KHCO3
- 6KHCO3 + Cr2(SO4)3 → 2Cr(OH)3↓ + 3K2SO4 + 6CO2↑
- 2Cr(OH)3 + 4NaOH + 3H2O2 → 2Na2CrO4 + 8H2O
Реальный ЕГЭ 2019. Задание 32. Вариант 10.
Смешали растворы сульфата калия и гидроксида бария. Выпавший осадок отделили, а через оставшийся раствор пропустили газ, полученный в результате взаимодействия серебра с концентрированной азотной кислотой. К образовавшемуся после пропускания газа раствору добавили водный раствор перманганата калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- K2SO4 + Ba(OH)2 → BaSO4↓ + 2KOH
- Ag + 2HNO3 → AgNO3 + NO2 + H2O
- 2NO2 + 2KOH → KNO2 + KNO3 + H2O
- 3KNO2 + 2KMnO4 + H2O → 2MnO2↓ + 2KOH + 3KNO3
Реальный ЕГЭ 2019. Задание 32. Вариант 11.
Алюминий прореагировал с раствором гидроксида натрия. К получившемуся раствору добавили избыток раствора азотной кислоты. Образовавшееся соединение алюминия выделили, высушили и прокалили. Полученную при этом газовую смесь пропустили через раствор гидроксида кальция. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑
- Na[Al(OH)4] + 4HNO3 → NaNO3 + Al(NO3)3 + 4H2O
- 4Al(NO3)3 → 2Al2O3 + 12NO2↑ + 3O2↑ (прокаливание)
- 2Ca(OH)2 + 2NO2 + 3O2 → 2Ca(NO3)2 + 2H2O
Реальный ЕГЭ 2019. Задание 32. Вариант 12.
Газ, полученный при обработке иодида калия концентрированной серной кислотой, сожгли в недостатке кислорода. Полученное при этом твёрдое вещество растворили в горячей концентрированной азотной кислоте. Выделившийся бурый газ пропустили через раствор гидроксида калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 8KI(тв.) + 9H2SO4(конц.) → 8KHSO4 + 4I2↓ + H2S↑ + 4H2O
- 2H2S + O2(недост.) → 2S↓ + 2H2O
- S + 6HNO3 → H2SO4 + 6NO2↑ + 2H2O
- 2NO2 + 2KOH → KNO2 + KNO3 + H2O
Реальный ЕГЭ 2019. Задание 32. Вариант 13.
Нитрат алюминия прокалили. Полученное твёрдое вещество поместили в раствор гидроксида калия. Через образовавшийся прозрачный раствор пропустили избыток газа, полученный при действии на бромид натрия концентрированной серной кислоты. При пропускании газа наблюдалось выпадение белого осадка. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 4Al(NO3)3 → 2Al2O3 + 12NO2↑ + 3O2↑ (прокаливание)
- Al2O3 + 2KOH + 3H2O → 2K[Al(OH)4]
- 8NaI(тв.) + 9H2SO4(конц.) → 8NaHSO4 + 4I2↓ + H2S↑ + 4H2O
- K[Al(OH)4] + H2S → KHS + Al(OH)3↓ + H2O
Реальный ЕГЭ 2019. Задание 32. Вариант 14.
Смесь газов, полученную при прокаливании нитрата меди(II), поглотили водой, при этом образовалась кислота. В горячий концентрированный раствор этой кислоты поместили оксид железа(II). Образовавшуюся соль железа выделили и поместили в раствор карбоната калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- 2Cu(NO3)2 → 2CuO + 4NO2 + O2↑ (прокаливание)
- 4NO2 + O2 + 2H2O → 4HNO3
- FeO + 4HNO3(конц.) → Fe(NO3)3 + NO2↑ + 2H2O
- 2Fe(NO3)3 + 3K2CO3 + 3H2O → 2Fe(OH)3↓ + 3CO2↑ + 6KNO3
Реальный ЕГЭ 2019. Задание 32. Вариант 15.
Фосфид калия растворили в воде. Через избыток образовавшегося раствора пропустили газ с неприятным запахом, полученный при действии на иодид калия концентрированной серной кислоты. К образовавшемуся после пропускания газа раствору добавили раствор сульфата алюминия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение- K3P + 3H2O → 3KOH + PH3↑
- 8KI(тв.) + 9H2SO4(конц.) → 8KHSO4 + 4I2↓ + H2S↑ + 4H2O
- 2KOH + H2S → K2S + 2H2O
- Al2(SO4)3 + 3K2S + 6H2O → 2Al(OH)3↓ + 3H2S↑ + 3K2SO4
Задание 33
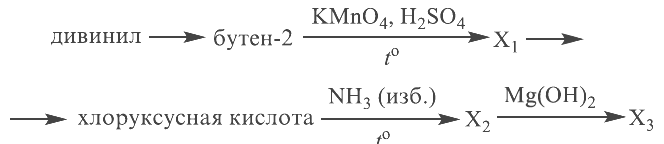
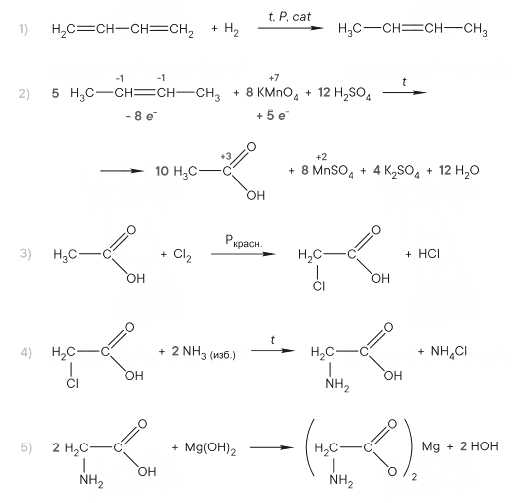
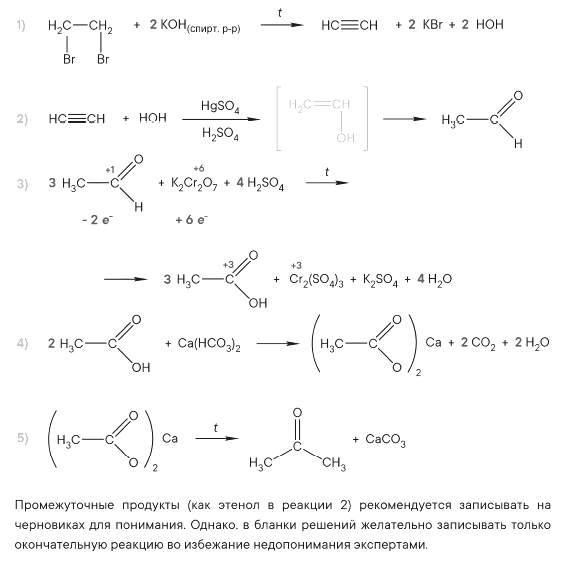
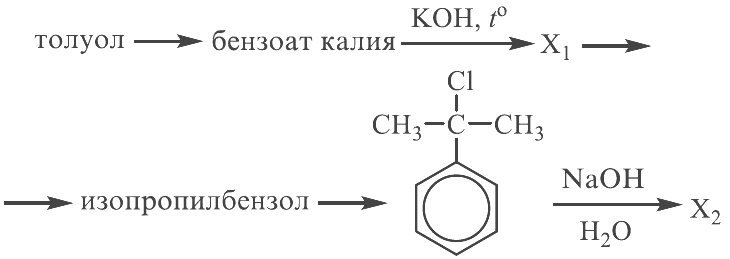
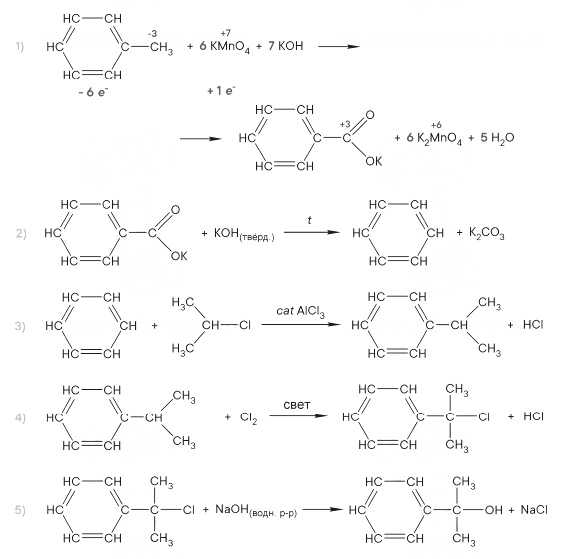
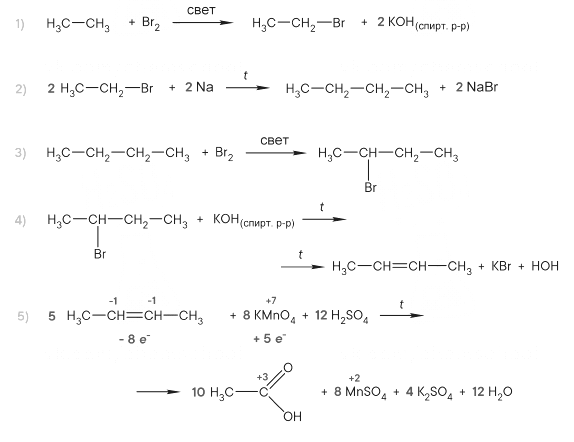
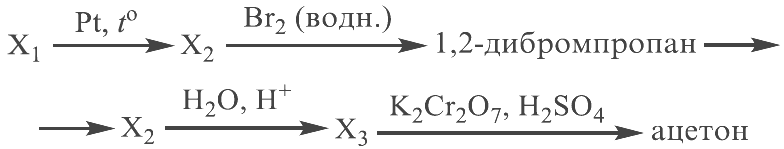
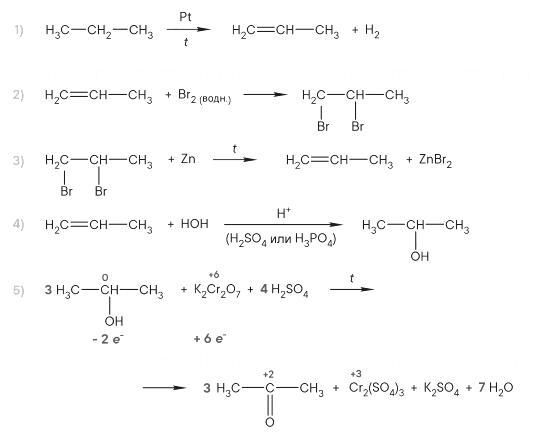
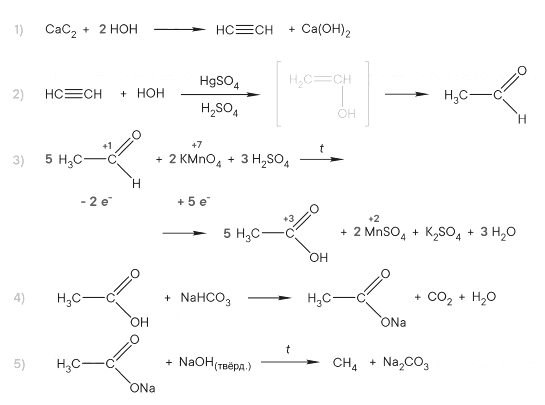
Реальный ЕГЭ 2019. Задание 33. Вариант 1.
Развернуть/свернуть решение
Реальный ЕГЭ 2019. Задание 33. Вариант 2.
Реальный ЕГЭ 2019. Задание 33. Вариант 3.
Реальный ЕГЭ 2019. Задание 33. Вариант 4.
Реальный ЕГЭ 2019. Задание 33. Вариант 5.
Реальный ЕГЭ 2019. Задание 33. Вариант 6.
Реальный ЕГЭ 2019. Задание 33. Вариант 7.
Реальный ЕГЭ 2019. Задание 33. Вариант 8.
Реальный ЕГЭ 2019. Задание 33. Вариант 9.
Реальный ЕГЭ 2019. Задание 33. Вариант 10.
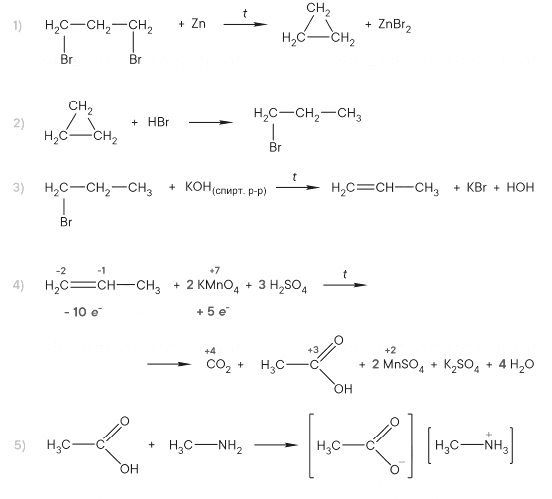
Развернуть/свернуть решение
Реальный ЕГЭ 2019. Задание 33. Вариант 11.
Развернуть/свернуть решение
Реальный ЕГЭ 2019. Задание 33. Вариант 12.
Развернуть/свернуть решение
Реальный ЕГЭ 2019. Задание 33. Вариант 13.
Развернуть/свернуть решение
Реальный ЕГЭ 2019. Задание 33. Вариант 14.
Развернуть/свернуть решение
Реальный ЕГЭ 2019. Задание 33. Вариант 15.
Развернуть/свернуть решение
Задание 34
Реальный ЕГЭ 2019. Задание 34. Вариант 1.
Растворимость безводного карбоната натрия при некоторой температуре составляет 31,8 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество карбоната натрия к 400 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора сульфата железа(III). К раствору во второй колбе добавили 300 г раствора азотной кислоты, также взятой в избытке. При этом, объём газа, выделившийся из второй колбы, оказался в 2 раза больше объёма газа, выделившегося из первой колбы. (Объёмы газов измерены при одинаковых условиях). Определите массовую долю нитрата натрия в конечном растворе во второй колбе.
Ответ: 22,1%.
Реальный ЕГЭ 2019. Задание 34. Вариант 2.
Растворимость безводного сульфида натрия при некоторой температуре составляет 15,6 г на 100 г воды. При этой температуре приготовили 289 г насыщенного раствора сульфида натрия. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора хлорида алюминия. К раствору во второй колбе добавили 100 г раствора соляной кислоты, также взятой в избытке. При этом, объём газа, выделившийся из второй колбы, оказался в 1,5 раза больше объёма газа, выделившегося из первой колбы. (Объёмы газов измерены при одинаковых условиях). Определите массовую долю хлорида натрия в конечном растворе во второй колбе.
Развернуть/свернуть решениеЭта задача аналогична задаче из Варианта 1, только химические уравнения другие, поэтому видео-объяснение вы можете посмотреть к задаче Варианта 1 и вы полностью поймёте, как решить эту задачу. Но для вашего удобства приведём очень подробное текстовое решение этой задачи:
1. Сначала запишем уравнения химических реакций, протекающих в колбах:
Колба 1: 3Na2S + 2AlCl3 + 6H2O = 2Al(OH)3↓ + 3H2S↑ + 6NaCl (уравнение 1)
Колба 2: Na2S + 2HCl = 2NaCl + H2S↑ (уравнение 2)
2. Определим то, что нужно найти в задаче и подробно распишем, как это найти через формулу массовой доли:
Найти нужно массовую долю хлорида натрия в конечном растворе во второй колбе. Значит надо подумать, как получился конечный раствор во второй колбе. Он получился добавлением к насыщенному раствору сульфида натрия, содержащегося во второй колбе, раствора соляной кислоты, за вычетом газа сероводорода (так как осадки и газы НЕ входят в состав раствора). Значит
W(в-ва) = m(в-ва)/m(р-ра)
W(NaCl) = m(NaCl)/m(р-ра Na2S из колбы 2) + m(p-pa HCl) — m(H2S образовавшегося в колбе 2)
3. Теперь мы должны найти каждый компонент в этой формуле по отдельности, всё подставить и найти ответ.
4. Чтобы найти массу NaCl, надо использовать уравнение 2, но никаких конкретных чисел для этого уравнения нет. Но известно по условию задачи, что «объём газа, выделившийся из второй колбы, оказался в 1,5 раза больше объёма газа, выделившегося из первой колбы». Т.е. уравнение 1 и 2 связаны через газ по химическому количеству (объём прямо пропорционален хим. количеству). Поэтому мы можем ввести х.
Пусть х моль газа выделилось в колбе 1, тогда 1,5х моль газа выделилось в колбе 2 (по условию задачи).
5. А связать эти переменные можно через Na2S, так как он есть и уравнении 1 и в уравнении 2, а также известно, что его раствор насыщенный и известна растворимость, значит мы можем найти общую массу, а затем и химическое количество сульфида натрия в исходной колбе (или, что тоже самое, сумму химических количеств Na2S в колбе 1 и колбе 2) с учётом того, что изначально приготовили 289 г насыщенного раствора.
Используем пропорцию для решения задач на растворимость (если вы не знакомы с задачами на растворимость, то смотрите отдельную страницу «Задачи на растворимость» с подробными видео-объяснениями)
| Соль | Вода | Раствор | |
| Растворимость | 15,6 г | 100 г | 115,6 г (15,6+100) |
| По условию задачи | y | 289 г |
Отсюда y=15,6 г*289 г/115,6 г = 39 г (Na2S исходный или общий).
n = m/M, M(Na2S) = 78 г/моль, n(Na2S) = 39г/78 г/моль = 0,5 моль
6. Теперь найдём химическое количество Na2S по уравнению 1 и по уравнению 2 через выделившийся газ Н2S. Сложим их и приравняем к общему хим. количеству Na2S, так как известно, что Na2S полностью прореагировал, потому что добавляемые растворы были в избытке (об этом сказано в условии задачи), и найдём х.
n(Na2S) = n(H2S) = x моль (по уравнению 1)
n(Na2S) = n(H2S) = 1,5 x моль (по уравнению 2)
х + 1,5х = 0,5
2,5 х = 0,5
х = 0,2
7. Теперь зная х, мы можем найти количестов NaCl по уравнению 2
n(NaCl) = 2n(H2S) = 2*1,5х = 3х = 3*0,2 моль = 0,6 моль (по уравнению 2)
m = n*M, M(NaCl) = 58,5 г/моль, m(NaCl) = 0,6 моль*58,5 г/моль = 35,1 г
8. Также мы можем найти массу улетевшего H2S из колбы 2
n(H2S) = 1,5x = 1,5*0,2 моль = 0,3 моль
m = n*M, M(H2S) = 34 г/моль, m(H2S) = 0,3 моль*34 г/моль = 10,2 г
9. И теперь находим массу раствора Na2S во второй колбе через растворимость
n(Na2S в колбе 2) = 1,5x = 1,5*0,2 моль = 0,3 моль
m = n*M, M(Na2S) = 78 г/моль, m(Na2S) = 0,3 моль*78 г/моль = 23,4 г
| Соль | Вода | Раствор | |
| Растворимость | 15,6 г | 100 г | 115,6 г (15,6+100) |
| По условию задачи | 23,4 г | z |
Отсюда z=23,4 г*115,6 г/15,6 г = 173,4 г (масса раствора Na2S во второй колбе)
10. Теперь всё подставим в формулу из пункта 2 и найдём ответ задачи:
W(NaCl) = m(NaCl)/m(р-ра Na2S из колбы 2) + m(p-pa HCl) — m(H2S образовавшегося в колбе 2) = 35,1 г/173,4 г + 100 г — 10,2 г = 35,1 г/263,2 г = 0,133 или 13,3%.
Ответ: 13,3%.
Реальный ЕГЭ 2019. Задание 34. Вариант 3.
Растворимость безводного хлорида алюминия при некоторой температуре составляет 53,4 г на 100 г воды. При этой температуре приготовили 306,8 г насыщенного раствора хлорида алюминия. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора карбоната калия. К раствору во второй колбе добавили 300 г раствора аммиака, также взятого в избытке. При этом, масса осадка, выпавшего во второй колбе, оказалась в 3 раза больше массы осадка, выпавшего в первой колбе. Определите массовую долю хлорида аммония в конечном растворе во второй колбе.
Реальный ЕГЭ 2019. Задание 34. Вариант 4.
Растворимость безводного карбоната аммония при некоторой температуре составляет 96 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество карбоната аммония к 250 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток твёрдого гидроксида натрия и нагрели до прекращения выделения газа. К раствору во второй колбе добавили 250 г раствора соляной кислоты, также взятой в избытке. При этом, объём газа, выделившийся из первой колбы, оказался в 3 раза больше объёма газа, выделившегося из второй колбы. (Объёмы газов измерены при одинаковых условиях). Определите массовую долю хлорида аммония в конечном растворе во второй колбе.
Развернуть/свернуть решениеЭта задача аналогична задаче из Варианта 1, только химические уравнения другие, поэтому видео-объяснение вы можете посмотреть к задаче Варианта 1 и вы полностью поймёте, как решить эту задачу. Но для вашего удобства приведём очень краткое текстовое решение этой задачи для вашей самопроверки.
1. Колба 1: (NH4)2CO3 + 2NaOH = Na2CO3 + 2NH3↑ + 2H2O (уравнение 1)
Колба 2: (NH4)2CO3 + 2HCl = 2NH4Cl + CO2↑ + H2O (уравнение 2)
2. W(в-ва) = m(в-ва)/m(р-ра)
W(NH4Cl) = m(NH4Cl)/m(р-ра (NH4)2CO3 из колбы 2) + m(p-pa HCl) — m(CO2)
3. Пусть х моль газа CO2 выделилось в колбе 2, тогда 3х моль газа NH3 выделилось в колбе 1 (по условию задачи).
4. Используем пропорцию для решения задач на растворимость (если вы не знакомы с задачами на растворимость, то смотрите отдельную страницу «Задачи на растворимость» с подробными видео-объяснениями)
| Соль | Вода | Раствор | |
| Растворимость | 96 г | 100 г | |
| По условию задачи | y | 250 г |
Отсюда y=96 г*250 г/100 г = 240 г ((NH4)2CO3 исходный или общий).
n = m/M, M((NH4)2CO3) = 96 г/моль, n((NH4)2CO3) = 240г/96 г/моль = 2,5 моль
5. n((NH4)2CO3) = 1/2n(NH3) = 1,5x моль (по уравнению 1)
n((NH4)2CO3) = n(CO2) = x моль (по уравнению 2)
1,5х + х = 2,5
2,5 х = 2,5
х = 1
6. n(NH4Cl) = 2n(CO2) = 2*х = 2*1 моль = 2 моль (по уравнению 2)
m = n*M, M(NH4Cl) = 53,5 г/моль, m(NH4Cl) = 2 моль*53,5 г/моль = 107 г
7. n(CO2) = x = 1 моль
m = n*M, M(CO2) = 44 г/моль, m(CO2) = 1 моль*44 г/моль = 44 г
8. n((NH4)2CO3 в колбе 2) = x = 1 моль
m = n*M, M((NH4)2CO3) = 96 г/моль, m((NH4)2CO3) = 1 моль*96 г/моль = 96 г
| Соль | Вода | Раствор | |
| Растворимость | 96 г | 100 г | 196 г |
| По условию задачи | 96 г | z |
Отсюда z=96 г*196 г/96 г = 196 г (масса раствора (NH4)2CO3 во второй колбе)
9. W(NH4Cl) = m(NH4Cl)/m(р-ра (NH4)2CO3 из колбы 2) + m(p-pa HCl) — m(CO2) = 107 г/196 г + 250 г — 44 г = 107 г/402 г = 0,266 или 26,6%
Ответ: 26,6%
Реальный ЕГЭ 2019. Задание 34. Вариант 5.
Растворимость безводного карбоната натрия при некоторой температуре составляет 31,8 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество карбоната натрия к 200 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора соляной кислоты. При этом выделилось 4,48 л (н.у.) газа. К раствору во второй колбе добавили 222 г 25%-ного раствора хлорида кальция. Определите массовую долю хлорида кальция в конечном растворе во второй колбе.
Реальный ЕГЭ 2019. Задание 34. Вариант 6.
Растворимость безводного сульфата железа(II) при некоторой температуре составляет 30,4 г на 100 г воды. При этой температуре приготовили 326 г насыщенного раствора сульфата железа(II). Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора хлорида бария. При этом образовалось 46,6 г осадка. К раствору во второй колбе добавили 50 г 34%-ного раствора аммиака. Определите массовую долю аммиака в конечном растворе во второй колбе.
Развернуть/свернуть решениеЭта задача аналогична задаче из Варианта 5, только химические уравнения другие, поэтому видео-объяснение вы можете посмотреть к задаче Варианта 5 (cмотри выше) и вы полностью поймёте, как решить эту задачу. Но для вашего удобства приведём очень краткое текстовое решение этой задачи для вашей самопроверки.
- Колба 1:FeSO4 + BaCl2 = BaSO4↓ + FeCl2 (уравнение 1)
Колба 2: FeSO4 + 2NH3 + 2H2O = Fe(OH)2↓ + (NH4)2SO4 (уравнение 2)
- W(в-ва) = m(в-ва)/m(р-ра)
W(NH3)конечн = m(NH3)исх – m(NH3)прор/m2(p-pa FeSO4) + m(p-pa NH3)исх – m(Fe(OH)2
- Используем пропорцию для решения задач на растворимость (если вы не знакомы с задачами на растворимость, то смотрите отдельную страницу «Задачи на растворимость» с подробными видео-объяснениями)
| Соль | Вода | Раствор | |
| Растворимость | 30,4 г | 100 г | 130,4 г (30,4 + 100) |
| По условию задачи | х | 326 г |
Отсюда х=30,4 г*326 г/130,4 г = 76 г (FeSO4 исходный или общий).
n = m/M, M(FeSO4) = 152 г/моль, n(FeSO4) = 76 г/152 г/моль = 0,5 моль
- n = m/M, M(BaSO4) = 233 г/моль, n(BaSO4) = 46,6 г/233 г/моль = 0,2 моль
n1(FeSO4) = n(BaSO4) = 0,2 моль (по уравнению 1)
- n2(FeSO4) = n(FeSO4)исх – n1(FeSO4) = 0,5 моль – 0,2 моль = 0,3 моль
m2(FeSO4) = 0,3 моль * 152 г/моль = 45,6 г
- 6.Используем пропорцию на растворимость
| Соль | Вода | Раствор | |
| Растворимость | 30,4 г | 100 г | 130,4 г |
| По условию задачи | 45,6 г | z |
Отсюда z=45,6 г*130,4 г/30,4 г = 195,6 г (масса раствора FeSO4 во второй колбе)
- m(NH3)исх = 50 г * 0,34 = 17 г
n = m/M, M(NH3) = 17 г/моль, n(NH3)исх = 17 г/17 г/моль = 1 моль
n(NH3)прор = 2*n2(FeSO4) = 2*0,3 моль = 0,6 моль (по уравнению 2)
m = n*M, m(NH3)прор = 0,6 моль * 17 г/моль = 10,2 г
- n2(FeSO4) = n(Fe(OH)2 = 0,3 моль (по уравнению 2)
m = n*M, M(Fe(OH)2) = 90 г/моль, m(Fe(OH)2) = 0,3 моль * 90 г/моль = 27 г
- W(NH3)конечн = m(NH3)исх – m(NH3)прор/m2(p-pa FeSO4) + m(p-pa NH3)исх – m(Fe(OH)2 = 17 г – 10,2 г/195,6 г + 50 г – 27 г = 6,8 г/218,6 г = 0,031 или 3,1%
Ответ: 3,1%
Реальный ЕГЭ 2019. Задание 34. Вариант 7.
Растворимость безводного сульфата алюминия при некоторой температуре составляет 34,2 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество сульфата алюминия к 300 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора аммиака. При этом образовалось 15,6 г осадка. К раствору во второй колбе добавили 320 г 25%-ного раствора гидроксида натрия. Определите массовую долю сульфата натрия в конечном растворе во второй колбе.
Реальный ЕГЭ 2019. Задание 34. Вариант 8.
Растворимость безводного карбоната натрия при некоторой температуре составляет 31,8 г на 100 г воды. При этой температуре приготовили 395,4 г насыщенного раствора карбоната натрия. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора нитрата кальция. При этом образовалось 50 г осадка. К раствору во второй колбе добавили 252 г 30%-ного раствора азотной кислоты. Определите массовую долю азотной кислоты в конечном растворе во второй колбе.
Развернуть/свернуть решениеЭта задача аналогична задаче из Варианта 5, только химические уравнения другие, поэтому видео-объяснение вы можете посмотреть к задаче Варианта 5 (cмотри выше) и вы полностью поймёте, как решить эту задачу. Но для вашего удобства приведём очень краткое текстовое решение этой задачи для вашей самопроверки.
- Колба 1: Na2CO3 + Ca(NO3)2 = CaCO3↓ + 2NaNO3 (уравнение 1)
Колба 2: Na2CO3 + 2HNO3 = 2NaNO3 + CO2↑ +H2O (уравнение 2)
- W(в-ва) = m(в-ва)/m(р-ра)
W(HNO3)конечн = m(HNO3)исх – m(HNO3)прор/m2(p-pa Na2CO3) + m(p-pa HNO3)исх – m(CO2)
- Используем пропорцию для решения задач на растворимость (если вы не знакомы с задачами на растворимость, то смотрите отдельную страницу «Задачи на растворимость» с подробными видео-объяснениями)
| Соль | Вода | Раствор | |
| Растворимость | 31,8 г | 100 г | 131,8 г (31,8 + 100) |
| По условию задачи | х | 395,4 |
Отсюда х=31,8*395,4/131,8 = 95,4 г (Na2CO3 исходный или общий).
n = m/M, M(Na2CO3) = 106 г/моль, n(Na2CO3) = 95,4 г/106г/моль = 0,9 моль
- n = m/M, M(СaСO3) = 100 г/моль, n(СaСO3) = 50 г/100 г/моль = 0,5 моль
n1(Na2CO3) = n(СaСO3) = 0,5 моль (по уравнению 1)
- n2(Na2CO3) = n(Na2CO3)исх – n1(Na2CO3) = 0,9 моль – 0,5 моль = 0,4 моль
m2(Na2CO3) = 0,4 моль * 106 г/моль = 42,4 г
6.Используем пропорцию на растворимость
| Соль | Вода | Раствор | |
| Растворимость | 31,8 г | 100 г | 131,8 г |
| По условию задачи | 42,4 г | z |
Отсюда z=42,4 г*131,8 г/31,8 г = 175,73 г (масса раствора Na2CO3 во второй колбе)
- m(HNO3)исх = 252 г * 0,3 = 75,6 г
n = m/M, M(HNO3) = 63 г/моль, n(HNO3)исх = 75,6 г/63 г/моль = 1,2 моль
n(HNO3)прор = 2*n2(Na2CO3) = 2*0,4 моль = 0,8 моль (по уравнению 2)
m = n*M, m(HNO3)прор = 0,8 моль * 63 г/моль = 50,4 г
- n2(Na2CO3) = n(СO2) = 0,4 моль (по уравнению 2)
m = n*M, M(СO2) = 44 г/моль, m(СO2) = 0,4 моль * 44 г/моль = 17,6 г
- W(HNO3)конечн = m(HNO3)исх – m(HNO3)прор/m2(p-pa Na2CO3) + m(p-pa HNO3)исх – m(CO2) = 75,6г – 50,4г/175,73г + 252г – 17,6г = 25,2г/410,13г = 0,061 или 6,1%
Ответ: 6,1%
Реальный ЕГЭ 2019. Задание 34. Вариант 9.
Растворимость безводного сульфата железа(II) при некоторой температуре составляет 30,4 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество сульфата железа(II) к 250 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора гидроксида натрия. При этом образовалось 18 г осадка. К раствору во второй колбе добавили 870 г 15%-ного раствора нитрата бария. Определите массовую долю нитрата бария в конечном растворе во второй колбе.
Развернуть/свернуть решениеЭта задача аналогична задаче из Варианта 5, только химические уравнения другие, поэтому видео-объяснение вы можете посмотреть к задаче Варианта 5 (cмотри выше) и вы полностью поймёте, как решить эту задачу. Но для вашего удобства приведём очень краткое текстовое решение этой задачи для вашей самопроверки.
- Колба 1:FeSO4 + 2NaOH = Fe(OH)2↓ + Na2SO4 (уравнение 1)
Колба 2: FeSO4 + Ba(NO3)2 = BaSO4↓ + Fe(NO3)2 (уравнение 2)
- W(в-ва) = m(в-ва)/m(р-ра)
W(Ba(NO3)2)конечн = m(Ba(NO3)2)исх – m(Ba(NO3)2)прор/m2(p-pa FeSO4) + m(p-pa Ba(NO3)2)исх – m(BaSO4)
- Используем пропорцию для решения задач на растворимость (если вы не знакомы с задачами на растворимость, то смотрите отдельную страницу «Задачи на растворимость» с подробными видео-объяснениями)
| Соль | Вода | Раствор | |
| Растворимость | 30,4 г | 100 г | |
| По условию задачи | х | 250 г |
Отсюда х=30,4 г*250 г/100 г = 76 г (FeSO4 исходный или общий).
n = m/M, M(FeSO4) = 152 г/моль, n(FeSO4) = 76 г/152 г/моль = 0,5 моль
- n = m/M, M(Fe(OH)2) = 90 г/моль, n(СaСO3) = 18 г/90 г/моль = 0,2 моль
n1(FeSO4) = n(Fe(OH)2) = 0,2 моль (по уравнению 1)
- n2(FeSO4) = n(FeSO4)исх – n1(FeSO4) = 0,5 моль – 0,2 моль = 0,3 моль
m2(FeSO4) = 0,3 моль * 152 г/моль = 45,6 г
- 6.Используем пропорцию на растворимость
| Соль | Вода | Раствор | |
| Растворимость | 30,4 г | 100 г | 130,4 г |
| По условию задачи | 45,6 г | z |
Отсюда z=45,6 г*130,4 г/30,4 г = 195,6 г (масса раствора FeSO4 во второй колбе)
- m(Ba(NO3)2)исх = 870 г * 0,15 = 130,5 г
n = m/M, M(Ba(NO3)2) = 261 г/моль, n(Ba(NO3)2)исх = 130,5 г/261 г/моль = 0,5 моль
n(Ba(NO3)2)прор = n2(FeSO4) = 0,3 моль (по уравнению 2)
m = n*M, m(Ba(NO3)2)прор = 0,3 моль * 261 г/моль = 78,3 г
- n2(FeSO4) = n(BaSO4) = 0,3 моль (по уравнению 2)
m = n*M, M(BaSO4) = 233 г/моль, m(BaSO4) = 0,3 моль * 233 г/моль = 69,9 г
- W(Ba(NO3)2)конечн = m(Ba(NO3)2)исх – m(Ba(NO3)2)прор/m2(p-pa FeSO4) + m(p-pa Ba(NO3)2)исх – m(BaSO4) = 130,5 г – 78,3 г/195,6 г + 870 г – 69,9 г = 52,2 г/995,7 г = 0,052 или 5,2%
Ответ: 5,2%.
Реальный ЕГЭ 2019. Задание 34. Вариант 10.
Растворимость безводного сульфида натрия при некоторой температуре составляет 15,6 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество сульфида натрия к 250 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора соляной кислоты. При этом выделилось 4,48 л (н.у.) газа. К раствору во второй колбе добавили 450 г 15%-ного раствора хлорида меди(II). Определите массовую долю хлорида меди(II) в конечном растворе во второй колбе.
Развернуть/свернуть решение- Колба 1:Na2S + 2HCl = 2NaCl + H2S↑ (уравнение 1)
Колба 2: Na2S + CuCl2 = CuS↓ + 2NaCl (уравнение 2)
- W(в-ва) = m(в-ва)/m(р-ра)
W(CuCl2)конечн = m(CuCl2)исх – m(CuCl2)прор/m2(p-pa Na2S) + m(p-pa CuCl2)исх – m(CuS)
- Используем пропорцию для решения задач на растворимость (если вы не знакомы с задачами на растворимость, то смотрите отдельную страницу «Задачи на растворимость» с подробными видео-объяснениями)
| Соль | Вода | Раствор | |
| Растворимость | 15,6 г | 100 г | |
| По условию задачи | х | 250 г |
Отсюда х = 15,6 г*250 г/100 г = 39 г (Na2S исходный или общий).
n = m/M, M(Na2S) = 78 г/моль, n(Na2S) = 39 г/78 г/моль = 0,5 моль
- n = V/Vm, n(H2S) = 4,48 л/22,4 л/моль = 0,2 моль
n1(Na2S) = n(H2S) = 0,2 моль (по уравнению 1)
- n2(Na2S) = n(Na2S)исх – n1(Na2S) = 0,5 моль – 0,2 моль = 0,3 моль
m2(Na2S) = 0,3 моль * 78 г/моль = 23,4 г
- 6.Используем пропорцию на растворимость
| Соль | Вода | Раствор | |
| Растворимость | 15,6 г | 100 г | 115,6 г |
| По условию задачи | 23,4 г | z |
Отсюда z = 23,4 г*115,6 г/15,6 г = 173,4 г (масса раствора Na2S во второй колбе)
- m(CuCl2)исх = 450 г * 0,15 = 67,5 г
n = m/M, M(CuCl2) = 135 г/моль, n(CuCl2)исх = 67,5 г/135 г/моль = 0,5 моль
n(CuCl2)прор = n2(Na2S) = 0,3 моль (по уравнению 2)
m = n*M, m(CuCl2)прор = 0,3 моль * 135 г/моль = 40,5 г
- n2(Na2S) = n(CuS) = 0,3 моль (по уравнению 2)
m = n*M, M(CuS) = 96 г/моль, m(CuS) = 0,3 моль * 96 г/моль = 28,8 г
- W(CuCl2)конечн = m(CuCl2)исх – m(CuCl2)прор/m2(p-pa Na2S) + m(p-pa CuCl2)исх – m(CuS) = 67,5 г – 40,5 г/173,4 г + 450 г – 28,8 г = 27 г/594,6 г = 0,045 или 4,5%
Ответ: 4,5%.
Реальный ЕГЭ 2019. Задание 34. Вариант 11.
Растворимость безводного хлорида кальция при некоторой температуре составляет 55,5 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество хлорида кальция к 160 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора карбоната натрия. При этом образовалось 30 г осадка. К раствору во второй колбе добавили 595 г 40%-ного раствора нитрата серебра. Определите массовую долю нитрата серебра в конечном растворе во второй колбе.
Развернуть/свернуть решение- Колба 1:CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl (уравнение 1)
Колба 2: CaCl2 + 2AgNO3 = 2AgCl↓ + Ca(NO3)2 (уравнение 2)
- W(в-ва) = m(в-ва)/m(р-ра)
W(AgNO3)конечн = m(AgNO3)исх – m(AgNO3)прор/m2(p-pa CaCl2) + m(p-pa AgNO3)исх – m(AgCl)
- Используем пропорцию для решения задач на растворимость (если вы не знакомы с задачами на растворимость, то смотрите отдельную страницу «Задачи на растворимость» с подробными видео-объяснениями)
| Соль | Вода | Раствор | |
| Растворимость | 55,5 г | 100 г | |
| По условию задачи | х | 160 г |
Отсюда х = 55,5 г*160 г/100 г = 88,8 г (CaCl2 исходный или общий).
n = m/M, M(CaCl2) = 111 г/моль, n(CaCl2) = 88,8 г/111 г/моль = 0,8 моль
- n = m/M, M(CaCO3) = 100 г/моль, n(CaCO3) = 30 г/100 г/моль = 0,3 моль
n1(CaCl2) = n(CaCO3) = 0,3 моль (по уравнению 1)
- n2(CaCl2) = n(CaCl2)исх – n1(CaCl2) = 0,8 моль – 0,3 моль = 0,5 моль
m2(CaCl2) = 0,5 моль * 111 г/моль = 55,5 г
- 6.Используем пропорцию на растворимость
| Соль | Вода | Раствор | |
| Растворимость | 55,5 г | 100 г | 155,5 г |
| По условию задачи | 55,5 г | z |
Отсюда z = 55,5 г*155,5 г/55,5 г = 155,5 г (масса раствора CaCl2 во второй колбе)
- m(AgNO3)исх = 595 г * 0,4 = 238 г
n = m/M, M(AgNO3) = 170 г/моль, n(AgNO3)исх = 238 г/170 г/моль = 1,4 моль
n(AgNO3)прор = 2*n2(CaCl2) = 2 * 0,5 моль = 1 моль (по уравнению 2)
m = n*M, m(AgNO3)прор = 1 моль * 170 г/моль = 170 г
- 2*n2(CaCl2) = n(AgCl) = 2 * 0,5 моль = 1 моль (по уравнению 2)
m = n*M, M(AgCl) = 143,5 г/моль, m(AgCl) = 1 моль * 143,5 г/моль = 143,5 г
- W(AgNO3)конечн = m(AgNO3)исх – m(AgNO3)прор/m2(p-pa CaCl2) + m(p-pa AgNO3)исх – m(AgCl) = 238 г – 170 г/155,5 г + 595 г – 143,5 г = 68 г/607 г = 0,112 или 11,2%.
Ответ: 11,2%.
Задание 35
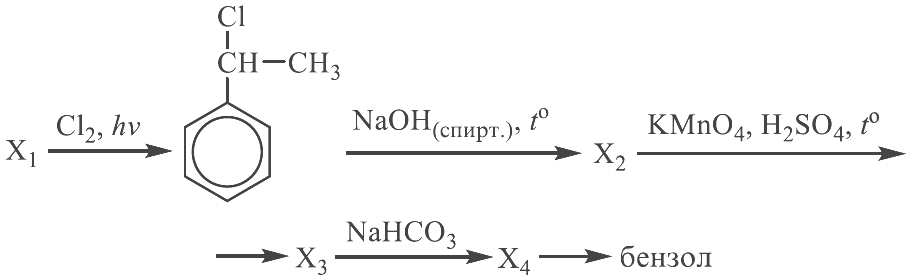
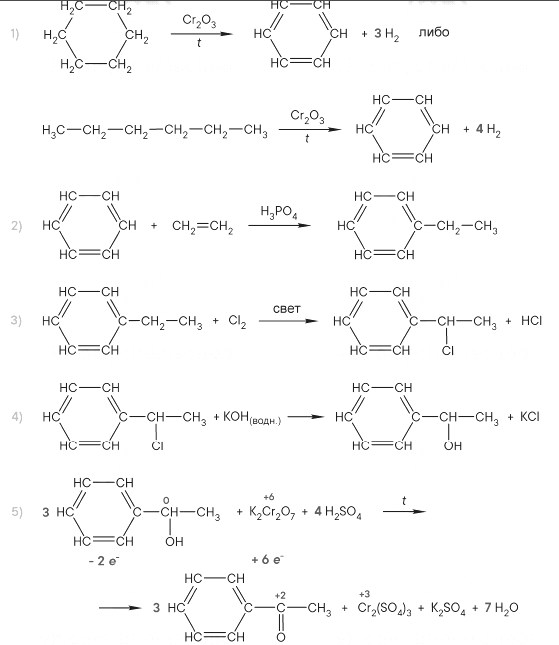
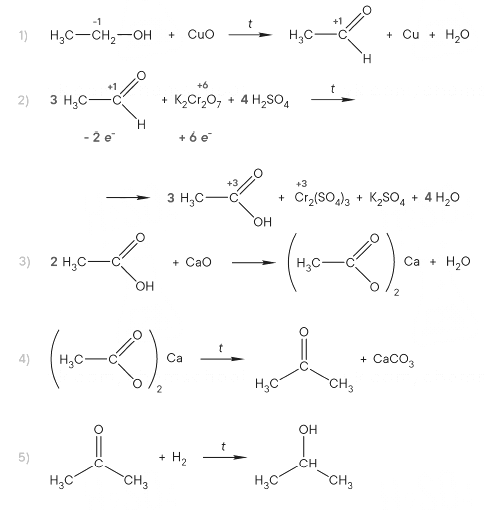
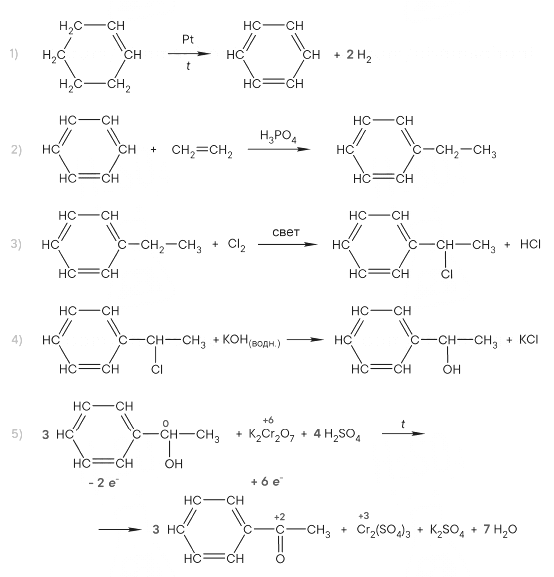
Реальный ЕГЭ 2019. Задание 35. Вариант 1.
Органическое вещество содержит 3,41% водорода, 34,09% углерода, 36,36% кислорода и 26,14 натрия по массе. Известно, что при нагревании этого вещества с избытком гидроксида натрия образуется предельный углеводород. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции, протекающей при нагревании исходного вещества с избытком гидроксида натрия.
Реальный ЕГЭ 2019. Задание 35. Вариант 2.
Органическое вещество, массовая доля углерода в котором равна 45,45%, водорода – 6,06%, кислорода – 48,48%, при нагревании реагирует с водным раствором гидроксида натрия, образуя два спирта и соль органической кислоты. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакциитисходного вещества с водным раствором гидроксида натрия.
Реальный ЕГЭ 2019. Задание 35. Вариант 3.
Органическое вещество, массовая доля углерода в котором равна 49,31%, кислорода – 43,84%, при нагревании реагирует с водным раствором гидроксида натрия, образуя этанол и соль органической кислоты. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции исходного вещества с водным раствором гидроксида натрия.
Решение этой задачи смотрите в следующем варианте, так как они абсолютно аналогичные.
Реальный ЕГЭ 2019. Задание 35. Вариант 4.
Органическое вещество, массовая доля водорода в котором равна 6,85%, кислорода – 43,84%, при нагревании реагирует с водным раствором гидроксида натрия, образуя этанол и соль органической кислоты. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции исходного вещества с водным раствором гидроксида натрия.
Реальный ЕГЭ 2019. Задание 35. Вариант 5.
Органическое вещество содержит 9,43% водорода, а также углерод и кислород, массовые доли которых равны. Известно, что это вещество реагирует с натрием и со свежеосажденным гидроксидом меди(II), молекула его содержит третичный атом углерода. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции исходного вещества с избытком натрия.
Реальный ЕГЭ 2019. Задание 35. Вариант 6.
При сжигании образца органического вещества массой 3,8 г получено 3,36 л (н.у.) углекислого газа и 3,6 г воды. Известно, что это вещество реагирует с натрием и со свежеосажденным гидроксидом меди(II). На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции исходного вещества с избытком азотной кислоты.
Реальный ЕГЭ 2019. Задание 35. Вариант 7.
Органическое вещество, массовая доля углерода в котором равна 40,68%, кислорода – 54,24%, при нагревании реагирует с водным раствором гидроксида натрия, образуя метанол и соль органической кислоты. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции исходного вещества с водным раствором гидроксида натрия.
Реальный ЕГЭ 2019. Задание 35. Вариант 8.
Органическое вещество содержит 2,47% водорода, 29,63% углерода, 39,5% кислорода и 28,4% натрия по массе. Известно, что при нагревании этого вещества с избытком гидроксида натрия образуется предельный углеводород. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции, протекающей при нагревании исходного вещества с избытком гидроксида натрия.
Реальный ЕГЭ 2019. Задание 35. Вариант 9.
При нагревании с водным раствором гидроксида натрия некоторое органические вещество подвергается гидролизу с образованием двух продуктов, первый из которых имеет состав С2H3O2Na. Второй продукт гидролиза содержит 38,71% углерода и 9,68% водорода по массе. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции гидролиза исходного вещества в растворе гидроксида калия.
Реальный ЕГЭ 2019. Задание 35. Вариант 10.
При сжигании образца органического вещества массой 8,76 г получено 8,064 л (н.у.) углекислого газа и 5,4 г воды. При нагревании в присутствии кислоты данное вещество подвергается гидролизу с образованием двух продуктов в соотношении 2 : 1, первый из которых имеет состав С2H4O2. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции гидролиза исходного вещества в кислой среде.
Реальный ЕГЭ 2019. Задание 35. Вариант 11.
При взаимодействии соли вторичного амина с ацетатом серебра образуется органическое вещество А и бромид серебра. Вещество А содержит 11,76% азота, 26,89% кислорода и 10,92% водорода по массе. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества А; 2) запишите молекулярную формулу органического вещества А; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции получения вещества А взаимодействием соли вторичного амина и ацетата серебра.
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ всех лет вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку



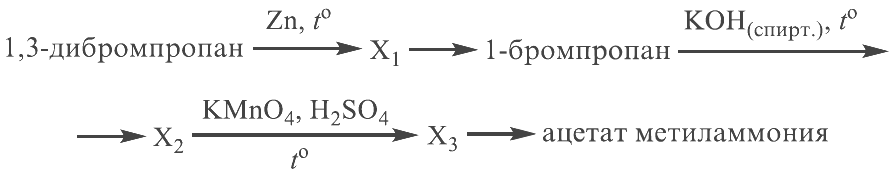


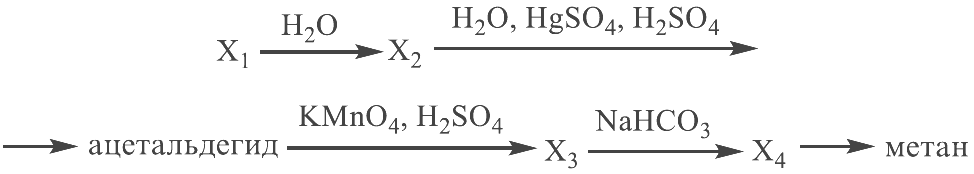




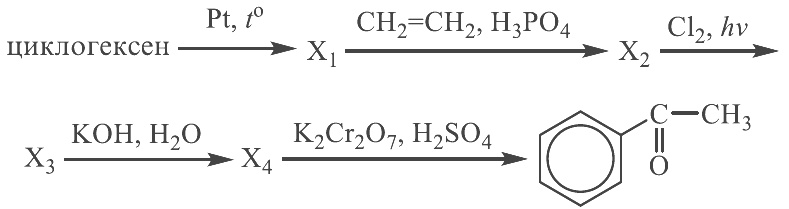
Здравствуйте, в задаче 34(2 вариант) при подсчете массы NaCl допущена ошибка. Вы пишите, что m(NaCl) = 0,6 моль*58,5 г/моль = 34,8 г, а должно быть 35,1
Здравствуйте. Вы правы, ошибку уже исправили! Спасибо за внимательность!
Задание 30 и 31. Вариант 2.
Возможна ли такая реакция?
Ag2S + HNO3 = Ag2SO4 + NO2 + H2O
Возможна для задания 30. Но в ЕГЭ 2019 её не засчитали, хотя потом признали её верной.
Задание 32, вариант 9. Вы написали такое уравнение реакции CO2 + KOH → KHCO3, но если избыток щелочи, то образуется средняя соль, а не кислая.
Здравствуйте. Спасибо за внимательность! Недочёт исправлен на избыток углекислого газа.