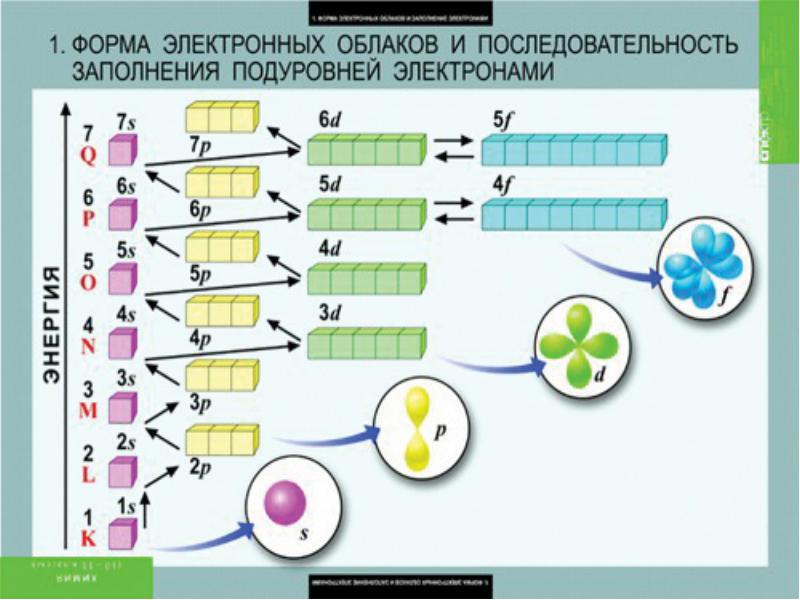
Закономерности распределения электронов по орбиталям
Подобно любой системе, атомы стремятся к минимуму энергии. Это достигается при определенном распределении электронов по орбиталям, которое можно оценить на основе таких закономерностей:
Принцип Паули: в атоме не может быть электронов с одинаковым значением всех четырех квантовых чисел.
Правило Гунда: электроны располагаются на одинаковых орбиталях таким образом, чтобы суммарный спин был максимален.
Правило Клечковского: порядок заполнения энергетических состояний определяется стремлением атома к минимальному значению суммы главного и побочного квантовых чисел, причем в пределах фиксированного значения n + l в первую очередь заполняются состояния, отвечающие минимальным значениям n.
Рассмотрим несколько примеров, поясняющих приведенные закономерности.
- Применение правила Клечковского для калия (Z = 19) и скандия (Z = 21).
Предшествующий калию элемент аргон (Z = 18) имеет следующее распределение электронов по орбиталям: 1s22s22p63s23p6.
При распределении электронов по орбиталям в атоме К в соответствии с правилом Клечковского предпочтение отдается орбитали 4s (сумма квантовых чисел n + l равна 4 + 0 = 4) по сравнению с орбиталью 3d (сумма квантовых чисел п + l равна 3 + 2 = 5), как орбитали, имеющей минимальное значение n + l
Следовательно, для атома К: 1s22s22p63s23p64s1
- Предшествующий скандию элемент кальций (Z = 20) имеет такое распределение электронов по орбиталям: 1s22s22p63s23p64s2
Из орбиталей 3d (n + l равно 3 + 2 = 5) и 4р (n + l равно 4 + 1 = 5) При распределении электронов в атоме Sc по орбиталям предпочтение следует отдать орбитали 3d, как орбитали, имеющей минимальное значение n = 3 при одинаковых суммах квантовых чисел n + l, равных 5.
Поэтому скандий характеризуется таким распределением электронов по орбиталям: 1s22s22p63s23p63d14s2
Примеры распределения электронов у элементов первых трёх периодов, а также калия и кальция:
Также вы можете посмотреть ВИДЕО-урок на эту тему:
И выполнить задания из ЦТ и ЕГЭ на эту тему вы можете здесь