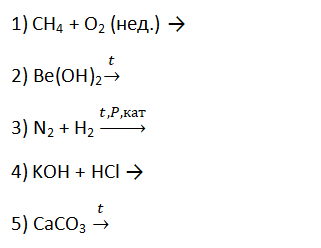Тесты по теме Основные классы неорганических веществ. Часть 8
Предлагаем вашему вниманию тесты по теме Основные классы неорганических веществ с подробными видео-объяснениями (даны сразу после условий задания) и ответами (приведены в конце страницы).
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
1. Нерастворимое основание образуется при взаимодействии:
1) AlCl3 (p-p) + NaOH (p-p, изб.)
2) BeO + H2O
3) Ba(OH)2 (p-p) + K2CO3
4) Cr(NO3)2 + LiOH (p-p, изб.)
2. В ряду Ag, CO2, Na2SO4, CaO, MgCO3 число веществ, которые реагируют с водным раствором ортофосфорной кислоты, составляет:
1) 2
2) 3
3) 4
4) 5
3. Укажите число возможных попарных взаимодействий между веществами HCl (р-р), HBr (р-р), F2, Fe (возможные реакции с водой НЕ учитывать):
1) 4
2) 3
3) 2
4) 5
4. При пропускании углекислого газа в пробирки с растворами веществ помутнение наблюдали в пробирках, содержащих:
а) Ca(OH)2;
б) Сa(HCO3)2;
в) Cu(NO3)2;
г) K2SiO3.
1) а, б
2) а, в
3) а, г
4) в, г
5. В отличие от соляной кислоты сероводородная кислота взаимодействует с:
1) ZnSO4
2) Ag
3) KOH
4) Cu(NO3)2
6. В водный раствор гидроксида цезия небольшими порциями добавляют оксид серы (IV). При этом сначала образуется:
1) сульфид цезия
2) сульфит цезия
3) гидросульфит цезия
4) надпероксид цезия
7. При приготовлении штукатурки для стен используют гашёную известь, которая реагирует с углекислым газом. В результате этого взаимодействия образуется:
1) оксид кальция
2) карбонат кальция
3) гидрокарбонат кальция
4) карбонат магния
8. Дана схема превращений
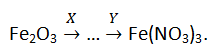 Все реации являются окислительно-восстановительными. Веществами Х и Y являются:
Все реации являются окислительно-восстановительными. Веществами Х и Y являются:
а) магний, конц. азотная кислота (t);
б) соляная кислота, нитрат серебра (I);
в) углерод, конц. азотная кислота (t);
г) угарный газ, оксид азота (V).
1) а, б
2) а, в
3) б, г
4) в, г
9. Несолеобразующий оксид может образоваться в результате реакции, схема которой:
10. Лакмус становится синим в растворе вещества, которое образуется по реакции замещения при смешении:
1) оксида кальция и раствора серной кислоты
2) оксида кальция и раствора хлорида натрия
3) оксида калия и соляной кислоты
4) серного ангидрида и воды
5) натрия и воды
11. С бромоводородом по реакции соединения реагирует:
1) K2CO3
2) Cu
3) NH3
4) ZnO
5) Cs
12. Укажите пару веществ, при смешении которых (электролиты представлены водными растворами) образуется средняя соль:
1) NaHCO3 + Ca(OH)2 (изб)
2) SO2 (изб) + KOH
3) H3PO4 (изб) + RbOH
4) H2SO4 (изб) + NH3 (p-p)
5) MgCO3 + CO2 (p-p)
13. Накипь удаляют с помощью:
1) раствора соды
2) раствора каменной соли
3) газообразного озона
4) раствора уксусной кислоты
5) твёрдой негашёной извести
14. Укажите схему, в результате которой образуются кислотный и основный оксиды: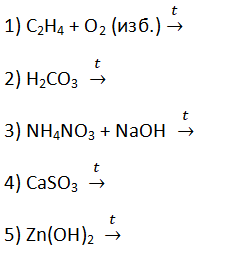
15. Укажите число оснований, которые можно получить в результате одностадийных попарных взаимодействий веществ CaO, Ba(OH)2, CuCl2, ZnO, H2O, Na (электролиты представлены водными растворами):
1) 1
2) 2
3) 3
4) 4
5) 5
16. Соли образуются по реакции соединения при взаимодействии:
а) HNO3 (p-p) и NH3;
б) H2SO3 и KOH (p-p, изб.);
в) ZnO и Na2O (сплавление);
г) Ca(HCO3)2 и NaOH (p-p);
д) K3PO4 (p-p) и H3PO4 (р-р, изб.);
е) CO2 (изб.) и Ba(OH)2 (p-p);
1) а, г, е
2) б, в, д
3) а, в, д, е
4) б, г, д, е
5) а, б
17. В схеме превращений,
веществами А и Б могут быть соответственно:
1) уксусная кислота и бромоводородная кислота
2) ацетат натрия и хлорид свинца (II)
3) ацетат кальция и гидроксид бария
4) ацетат серебра (I) и гидроксид натрия
5) ацетат серебра (I) и сульфат натрия
18. Выберите верные утверждения:
а) НЕгашеную известь можно получить разложением известняка;
б) сырьё для получения цемента – известняк и глина;
в) для получения легкоплавкого стекла вместо соды используют поташ;
г) формула мрамора – CaSiO3;
д) K2SiO3 встречается в природе в виде песка, кремнезёма и кварца.
1) а, б, в
2) а, г, д
3) б, г
4) б, в, д
5) в, г
19. С разбавленной бромоводородной кислотой при н.у. реагируют все оксиды в ряду:
1) CO2, CuO
2) SiO, BeO
3) Cs2O, Cr2O3
4) BaO, P2O5
5) NO, FeO
20. Cu(OH)2 можно получить при взаимодействии (электролиты находятся в виде водных растворов):
1) хлорида меди (II) и гидроксида железа (II)
2) оксида меди (I) и гидроксида калия
3) сульфида меди (II) и гидроксида бария
4) меди и гидроксида рубидия
5) сульфата меди (II) и гидроксид натрия
Ответы:
-
4
-
1
-
4
-
3
-
4
-
2
-
2
-
2
-
1
-
5
-
3
-
1
-
4
-
4
-
3
-
3
-
4
-
1
-
3
-
5
Также предлагаем вам сборку видео-уроков на эту тему:
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Посмотреть видео-объяснения каждого задания ЦТ, РТ и ДРТ всех лет, а также получить условия всех пробных, тренеровочных и реальных вариантов ЕГЭ, вы можете получив полный доступ к сайту кликнув здесь «Получить все материалы сайта»
А также:
- Просмотреть все тесты по органической химии
- Просмотреть все тесты по неорганической химии
- Посмотреть пробные варианты ЦТ вы можете здесь, нажав на эту строку
- Посмотреть пробные и реальные варианты ЕГЭ вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Больше заданий РТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЦТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЕГЭ вы можете найти здесь, нажав на эту строку
- Все видео-объяснения вы можете найти на YouTube канале, нажав на эту строку