Предлагаем вашему вниманию девятый пробный вариант РТ по химии 2020/2021 для подготовки к ЦТ по химии 2021, ответы представлены в конце страницы.
Скачать РТ по химии 2020/2021. Пробный вариант 9
ВНИМАНИЕ: все задания составлены автором самостоятельно и не являются копией заданий ЦТ и РТ. Если вам необходимы оригинальные задания, то вам надо записываться на этапы РТ (на сайте РИКЗ) и покупать сборники реальных заданий ЦТ и РТ в книжных магазинах.
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
Вариант 9
Для получения полного доступа к сайту переходите по ссылке: http://www.yoursystemeducation.com/poluchit-video/. В полном доступе вы найдёте условия и видео-объяснения заданий-аналогов из всех этапов РТ начиная с 2014 года, а также всех заданий-аналогов ЦТ начиная с самого первого ЦТ 2004 года.
Вариант содержит 44 задания и состоит из части А (28 заданий) и части В (16 заданий). На выполнение всего теста отводится 150 минут. Необходимые справочные материалы – «Периодическая система химических элементов Д.И. Менделеева», «Растворимость кислот, оснований и солей в воде», Электрохимический ряд активности металлов» — приведены в конце теста.
При расчётах принять молярный объём газа (Vm) 22,4 дм3/моль. Значения относительных атомных масс химических элементов (кроме хлора, для которого Ar = 35,5) следует округлять до целого числа. При решении заданий можно пользоваться микрокалькулятором.
Часть А
Для получения приближённого значения чисел в промежуточных расчётах округлите их до третьего знака после запятой по правилам округления. Конечный результат округлите, ориентируясь на числа, предложенные в ответе.
В каждом задании только ОДИН из предложенных вариантов ответа является верным.
А1. Во втором периоде периодической системы число химических элементов металлов и неметаллов соответственно равно:
1) 2 и 6
2) 6 и 2
3) 3 и 5
4) 5 и 3
5) 1 и 7
А2. Электронная конфигурация атома в основном состоянии 1s22s22p2. Число спаренных и неспаренных электронов в атоме равно соответственно:
1) 4 и 0
2) 4 и 2
3) 2 и 0
4) 2 и 2
5) 3 и 0
А3. У элементов IA группы с увеличением атомного номера:
1) усиливаются основные свойства гидроксидов
2) уменьшается степень окисления окисления атомов в простых веществах
3) увеличивается степень окисления в высшем оксиде
4) радиус атома последовательно уменьшается
5) ослабевают восстановительные свойства атомов
А4. Вставьте пропуски в предложении – из веществ вода, сероводород, селеноводород наибольшую температуру кипения имеет ……, так как обладает …….:
1) H2O, меньшей длиной связи
2) H2S, большей длиной связи
3) H2O, водородными связями между молекулами
4) H2Se, большим размером молекулы
5) H2Se, молекулярной кристаллической решёткой в твёрдом агрегатном состоянии
А5. Степень окисления -1 имеют атомы одного из элементов в веществе:
1) Cl2O
2) H2Te
3) PH3
4) SrO
5) CaO2
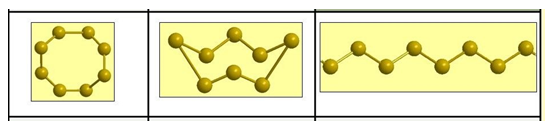
А6. На рисунке представлены структуры веществ, образованных элементом:
2) кислород
3) фосфор
4) сера
5) хлор
А7. Имеется смесь газов объёмом 5,6 дм3 (н.у.), которая имеет молярную массу 36 г/моль. Масса (г) этой смеси составляет:
1) 6,43
2) 9
3) 144
4) 201,6
5) 806,4
А8. Правильно составлена пара: класс – название представителя:
1) кислотный оксид – оксид серы (IV)
2) основный оксид – оксид хрома (VI)
3) солеобразующий оксид – оксид кремния (II)
4) амфотерный оксид – оксид железа (II)
5) несолеобразующий оксид – оксид азота (IV)
А9. Выберите НЕВЕРНОЕ утверждение, характеризующее гидроксид железа (III):
1) при нагревании превращается в один из оксидов железа
2) массовая доля водорода в гидроксиде составляет 3%
3) является растворимым основанием
4) при нагревании реагирует с гидроксидом калия
5) имеет ионную кристаллическую решётку
А10. Даны вещества: Pb(NO3)2 (p-p), NO2 (воздух), N2O, H2O, AgNO3 (p-p), HCl (p-p), NaCl (тв), Ba(OH)2. Укажите количество попарных взаимодействий этих веществ, в результате которых образуется азотная кислота:
1) 2
2) 3
3) 4
4) 5
5) 6
А11. Укажите название вещества, которое можно использовать для осушки газа хлороводород:
1) гидроксид калия
2) гашёная известь
3) нитрат серебра
4) оксид серы (IV)
5) оксид фосфора (V)
А12. Концентрированная серная кислота в отличие от разбавленной может реагировать с:
1) раствором нитрата бария и раствором гидроксида натрия
2) твёрдым нитратом калия и твёрдым хлоридом калия
3) твердым карбонатом кальция и твердым сульфидом цинка
4) раствором хлорида кальция и твёрдым гидрокарбонатом лития
5) раствором нитрата свинца (II) и раствором гидроксида стронция
А13. Азот в отличие от фосфора:
1) является питательным элементом и входит в состав комплексных удобрений
2) в соединениях с металлами проявляет отрицательную степень окисления
3) содержится в выдыхаемом человеком воздухе
4) в молекуле простого вещества НЕ содержит кратные связи
5) образует только одну кислородсодержащую кислоту
А14. Помутнение наблюдается при пропускании углекислого газа через растворы:
1) K2CO3 и Ca(OH)2
2) K2CO3 и Zn(HCO3)2
3) Ba(NO3)2 и Ca(OH)2
4) Ba(NO3)2 и Zn(HCO3)2
5) Ca(OH)2 и Zn(HCO3)2
А15. Укажите ответ, в котором первое вещество обуславливает жёсткость воды, а втрое – устраняет её:
1) CaSO4, HCl
2) MgSO4, NaHCO3
3) Na2SO4, Mg(HCO3)2
4) Mg(HCO3)2, NaOH
5) CaCO3 и CO2
А16. Дана схема превращений ![]() Первая реакция относится к реакциям замещения, вторая и третья – обмена. Укажите зашифрованные вещества соответственно:
Первая реакция относится к реакциям замещения, вторая и третья – обмена. Укажите зашифрованные вещества соответственно:
1) азотная кислота, сероводород, сульфат калия
2) нитрат ртути (II), сероводород, серная кислота
3) оксид азота (IV), сульфид калия, оксид серы (VI)
4) нитрид лития, сера, серная кислота
5) нитрат ртути (II), сульфид калия, серная кислота
А17. Укажите вещества, при взаимодействии которых соединения алюминия будут проявлять кислотные свойства:
а) оксид алюминия и углекислый газ;
б) гидроксид алюминия и соляная кислота;
в) оксид алюминия и водный раствор гидроксида цезия;
г) гидроксид алюминия и гидроксид калия;
1) а, б
2) а, в
3) б, г
4) а, г
5) в, г
А18. Наибольшей электропроводностью обладает раствор (молярные концентрации всех растворов равны):
1) HI
2) H2SO3
3) HF
4) C2H5COOH
5) NH3
А19. Имеется сокращённое ионное уравнение Mg2+ + CO32- = MgCO3. Укажите ионы присутствующие в полном ионном уравнении:
1) OH— и K+
2) Cl— и Ba2+
3) SO42- и Na+
4) OH— и H+
5) Br— и Ca2+
А20. В растворе протекает гомогенная окислительно-восстановительная реакция: 2А + 2Б = 3В + 2Г. На рисунке приведён график зависимости молярной концентрации вещества А от времени. По этим данным безусловно можно утверждать, что:
 1) скорость образования вещества Г в 1,5 раза меньше, чем скорость образования вещества В
1) скорость образования вещества Г в 1,5 раза меньше, чем скорость образования вещества В
2) концентрация А со временем увеличивается
3) реакция является эндотермической
4) вещество А расходуется медленнее, чем вещество Б
5) скорость этой реакции независит от концентрации исходных веществ
А21. Пространственные изомеры существуют у:
1) пропен и 3-бромпропен-1
2) 2-бромбутен-2 и 1-бромбутадиен-1,3
3) 2-бромбутен-2 и 3-бромпропен-1
4) 1-бромбутадиен-1,3 и 3-бромпропен-1
5) пропен и 1-бромбутадиен-1,3
А22. Плотность паров изопрена по дивинилу равна:
1) 0,67
2) 0,79
3) 1,26
4) 1,54
5) 2,01
А23. В отличие от фенола бензол:
1) реагирует при определённых условиях с водородом
2) реагирует со щелочами
3) относится к ароматическим соединениям
4) является при 10С жидким веществом
5) реагирует с кислородом воздуха при нагревании
А24. Укажите пару веществ, с помощью которых по отдельности можно различить водные растворы этиленгликоля и формальдегида:
1) оксид меди (I), бензол
2) разбавленная серная кислота, этанол
3) гидроксид натрия, ацетон
4) аммиачный раствор оксида серебра (I), гидроксид меди (II)
5) вода, уксусная кислота
А25. Массовые доли углерода и кислорода в карбоновой кислоте равны соответственно 26,09% и 69,57%. Выберите схему получения этой кислоты:
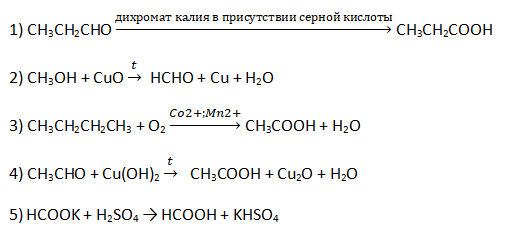 А26. Укажите продукты реакции C12H22O11 + H2O :
А26. Укажите продукты реакции C12H22O11 + H2O :
1) 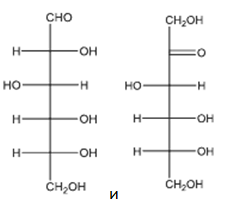 2)
2) 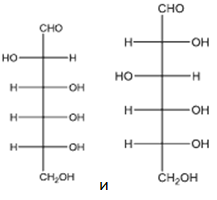 3)
3) 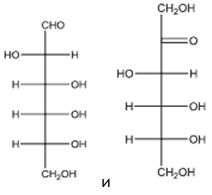 4)
4) 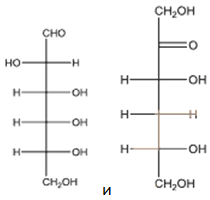 5)
5) 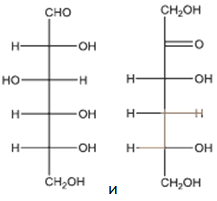 А27. Укажите название органического вещества, которое реагирует и с кислотами и со щелочами:
А27. Укажите название органического вещества, которое реагирует и с кислотами и со щелочами:
1) валин
2) метиламин
3) фенол
4) этанол
5) глицерин
А28. Укажите пару, в которой даны названия полиамидного и полиэфирного волокон соответственно:
1) вискоза и лавсан
2) полиэтилен и капрон
3) капрон и лавсан
4) полиизопрен и ацетатное волокно
5) тефлон и целлюлоза
Часть В
При решении задач в промежуточных расчётах для получения приближенного значения чисел округлите их до третьего знака после запятой по правилам округления, а конечный результат – до целого числа. Единицы измерения числовых величин не указывайте.
В1. Установите соответствие между формулой органического вещества и формулой его гомолога.
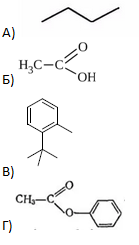 |
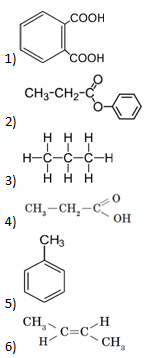 |
Ответ запишите в виде сочетания букв и цифр, например: А2Б1В5Г3.
В2. Выберите утверждения, характеризующие этилен / ацетилен соответственно:
1) в составе молекулы имеется: двойная связь / тройная связь;
2) по номенклатуре ИЮПАК имеет название: этин / этен;
3) длина связи между атомами углерода составляет (нм): 0,133 / 0,120;
4) плотность (н.у.) составляет (г/дм3) : 1,25 / 1,16;
5) фитогормон, ускоряющий созревание плодов / используется для газовой сварки и резки металлов;
6) молекулы имеют: линейное строение / плоскостное строение;
Ответ запишите в виде последовательности цифр в порядке возрастания, например 1235
В3. Укажите молярную массу (г/моль) хлоросодержащего органического вещества Д, который образуется в результате превращения:
 В4. Выберите верные утверждения о кислороде:
В4. Выберите верные утверждения о кислороде:
1) не имеет цвета во всех агрегатных состояниях;
2) все бинарные соединения с кислородом относятся к классу оксидов;
3) атомы кислорода представлены стабильными изотопами О-16, О-17, О-18 и кислород образует две аллотропные модификации простых веществ;
4) может проявлять степени окисления -2, -1, 0, +2;
5) валентность всегда равна II;
6) является самым распространённым элементом на нашей планете;
7) в реакции со фтором проявляет восстановительные свойства.
Ответ укажите в виде последовательности цифр, например 1256.
В5. Подсолнечное масло массой 10 г обесцвечивает раствор брома в тетрахлористом углероде массой 120 г с массовой долей брома 18%. Рассчитайте объём (н.у.) водорода в дм3, который необходим для полного гидрирования данного масла, если в результате гидрирования образуется продукт массой 1,5 кг.
В6. Определите сумму молярных масс (г/моль) цинкосодержащего вещества В, хлорсодержащего вещества Е и азотсодержащего вещества З, образующихся в результате превращений:
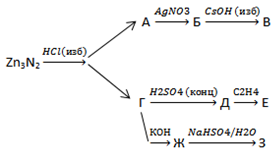 В7. Укажите соответствие между веществом и парой веществ, из которых можно получить это вещество (электролиты представлены разбавленными водными растворами).
В7. Укажите соответствие между веществом и парой веществ, из которых можно получить это вещество (электролиты представлены разбавленными водными растворами).
| А) AgCl
Б) K2[Be(OH)4] В) Ca(NO3)2 Г) CuSO4 |
1. KCl + Be(OH)2
2. Cu(OH)2 + H2SO4 3. CaO + HNO3 4. Be + KOH 5. AgNO3 + NaCl 6. CaCO3 + NaNO3 7. Ag + HCl 8. CuCl2 + K2SO4 |
Ответ запишите в виде сочетания букв и цифр, например: А2Б2В5Г3.
В8. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции (электролиты представлены разбавленными водными растворами).
| А) NaF и MgCl2
Б) Al(OH)3 и KOH В) HCl и K2S Г) Al4C3 и HBr |
1. Выделение газа без запаха
2. Выделение газа с неприятным запахом 3. Выпадение осадка 4. Растворение осадка 5. Изменение окраски раствора |
Ответ запишите в виде сочетания букв и цифр, например: А2Б1В5Г3.
В9. Установите соответствие между способом воздействия на равновесную систему
H2Se (г) + H2O (ж) ↔ H+ (p-p) + HSe— (p-p) + Q,
и направлением смещения химического равновесия при этом воздействии.
| А) повышение давления
Б) понижение температуры В) добавление твёрдого селенида аммония Г) добавление щёлочи |
1. Практически не смещается
2. Смещается вправо 3. Смещается влево |
Ответ запишите в виде сочетания букв и цифр, например: А3Б2В3Г3 (цифры могут повторяться).
В10. Бинарное твёрдое вещество А разлагается водой с образованием ядовитого газа Б и щёлочи В. Воспламенение газа Б на воздухе приводит к образованию соединения Г, что обусловливает появление блуждающих огней на старых кладбищах. Соединение Г взаимодействует с веществом В, образуя вещество Д, которое является составной частью минерала апатита. Установите соответствие между зашифрованным веществом и его молярной массой (г/моль).
| А
Б В Г Д |
1. 182
2. 310 3. 136 4. 98 5. 74 6. 34 |
Ответ запишите в виде сочетания букв и цифр, например: А2Б4В5Г3Д1.
В11. Установите соответствие между названием лабораторного оборудования и его применением.
| А. Лабораторный штатив
Б. Колба коническая В. Ступка с пестиком Г. Металлический шпатель Д. Мензурка |
1) хранение жидких веществ или растворов
2) измельчение твёрдых веществ 3) упаривание растворов 4) закрепление пробирок и колб 5) для измерения объёма жидкости 6) для взятия небольших порций сыпучих веществ |
Ответ запишите в виде сочетания букв и цифр, например: А1Б2В5Г3Д4.
В12. Смесь кислорода с водородом в отношении химических количеств 1:3 соответственно подожгли. Полученную газовую смесь оставили при постоянной температуре в 100С. При этом относительная плотность по водороду возросла на 11%. Укажите выход (%) продукта реакции.
В13. Массовая доля трёхвалентного металла в смеси, состоящей из его оксида и гидроксида, составляет 45%. Химические количества веществ равны между собой. Укажите молярную массу (г/моль) металла.
В14. Разложение сульфита бария протекает согласно термохимическому уравнению:
BaSO3 (т) = BaO (т) + SO2 (г) – 599,04 кДж.
Для разложения образца сульфита бария необходимо 46,8 кДж теплоты. Выделившейся при этом газ был полностью поглощён раствором гидроксида натрия массой 160 г с массовой долей щёлочи 1,75%. Рассчитайте массовую долю (%) соли в полученном растворе.
В15. В раствор объёмом 2 дм3 с плотностью 1,02 г/см3 с массовой долей гидроксида лития 24% опустили кусочек металлического лития массой 21 г. Укажите массу (г)щёлочи в образовавшемся растворе.
В16. Смесь лития, натрия и рубидия массой 20 г растворили в иодоводородной кислоте массой 300 г с массовой долей HI 24%. После окончания реакции получившийся раствор выпарили. Масса твёрдого остатка составила 83,5 г. Рассчитайте объём (дм3) выделившегося при этом водорода.
Ответы:
Часть А
- 1
- 2
- 1
- 3
- 5
- 4
- 2
- 1
- 3
- 2
- 5
- 2
- 3
- 3
- 4
- 5
- 5
- 1
- 3
- 1
- 2
- 3
- 4
- 4
- 5
- 1
- 1
- 3
Часть В:
- А3Б4В5Г2
- 1345
- 137
- 3467
- 442
- 596
- А5Б4В3Г2
- А3Б4В2Г1
- А2Б2В1Г2
- А1Б6В5Г4Д2
- А4Б1В2Г6Д5
- 40
- 27
- 4
- 562
- 6
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
Посмотреть видео-объяснения каждого задания ЦТ, РТ и ДРТ всех лет вы можете получив полный доступ к сайту кликнув здесь «Получить все материалы сайта»
- Посмотреть все пробные варианты ЦТ 2021 вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Больше заданий РТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЦТ вы можете найти здесь, нажав на эту строку
- Наш канал на YouTube вы можете посмотреть, нажав на эту строку