Скачать Пробный вариант 9. ЕГЭ 2021 по химии с ответами в формате pdf
Ответы вы найдёте в конце страницы
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
Часть 1
Ответом к заданиям 1–26 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Цифры в ответах на задания 5, 8, 9, 11, 16, 17, 21–26 могут повторяться.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
1) Cа 2) К 3) Р 4) Cl 5) F
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
- Укажите элементы, которые образуют только ионы, которые содержат больше протонов, чем электронов.
Запишите номера выбранных элементов.
- Из указанных в ряду химических элементов выберите три элемента, находящихся в малых периодах периодической системы. Расположите выбранные элементы в порядке уменьшения окислительной способности их атомов.
Запишите номера выбранных элементов в нужной последовательности.
- Из указанных в ряду элементов выберите два элемента, которые в соединениях могут проявлять степень окисления +5.
Запишите номера выбранных элементов.
- Из предложенного перечня выберите два пары веществ, в которых каждое из веществ не проводит ток и плавится при низкой температуре.
1) гептан и натрат кальция
2) фтор и кислород
3) оксид серы (IV) и сульфит калия
4) железо и сульфид калия
5) хлор и метан
Запишите номера выбранных веществ.
- Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
| КЛАСС/ГРУППА | НАЗВАНИЕ ВЕЩЕСТВА |
| А) простое вещество металл | 1) пероксид водорода |
| Б) простое вещество неметалл | 2) озон |
| В) неорганическое сложное вещество | 3) калий |
| 4) уксусная кислота | |
| 5) пропанон |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня веществ выберите два, которые реагируют с кремнием в соответствующих условиях.
1) Ca
2) H2
3) HBr (p-p)
4) CO2
5) KOH (p-p)
Запишите номера выбранных веществ.
- В двух пробирках находился раствор сульфида аммония. В первую пробирку добавили раствор вещества Х, а во вторую – раствор сильного электролита Y. В результате в первой пробирке наблюдалось выпадение чёрного осадка, во второй при нагревании – выделение газа, окрашивающего влажную лакмусовую бумажку в синий цвет. Из предложенного перечня выберите вещества Х и Y, которые могут вступить в описанные реакции.
1) Cu(OH)2
2) (CH3COO)2Pb
3) KOH
4) HCl
5) CaBr2
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) Cl2 | 1) Fe2O3, H2, NaOH |
| Б) ZnO | 2) HCl, CuO, СO2 |
| В) Mg | 3) NaOH, S, FeCl2 |
| Г) CO | 4) Na2CO3, NaBr , H2O |
| 5) HF, CaO, KOH |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами в этой реакции: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) Cr + H2SO4 (разб.) → | 1) CrSO4 + H2 |
| Б) Cr2O3 + H2SO4 → | 2) Cr2(SO4)3 + H2O |
| В) Na2CrO4 + H2SO4 (конц.) → | 3) Cr2(SO4)3 + SO2 + H2O |
| Г) Na[Cr(OH)4] + H2SO4 → | 4) Cr2(SO4)3 + Na2SO4 + H2O |
| 5) Cr2(SO4)3 + Na2SO4 + SO2 + H2O | |
| 6) Na2Cr2O7 + Na2SO4 + H2O |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана следующая схема превращений:
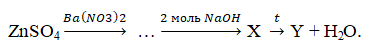 Определите, какие из указанных веществ являются веществами Х и Y.
Определите, какие из указанных веществ являются веществами Х и Y.
1) гидроксид цинка
2) гидроксид бария
3) оксид цинка
4) тетрагидроксоцинкат натрия
5) оксид бария
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
А) 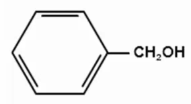 |
1) фенолы |
Б) 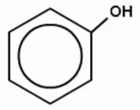 |
2) ароматические спирты |
В) 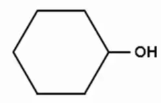 |
3) циклоалкенолы |
| 4) алициклические спирты |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня выберите две пары веществ, в каждой из которой вещества являются изомерами между србой.
1) цис-октен-2 и транс-октен-3
2) этиленгликоль и глицерин
3) этен и ацетилен
4) бутан и циклобутан
5) пропин и циклопропен
Запишите номера выбранных веществ.
- Из предложенного перечня выберите два вещества, которые не подвергаются гидрированию.
1) циклопропан
2) 2-метилбуталиен-1,3
3) 2-хлорпропан
4) ацетилен
5) декан
Запишите номера выбранных веществ.
- Из предложенного перечня выберите два вещества, которые взаимодействуют с водным раствором перманганата калия.
1) уксусная кислота
2) 2-метилпропанол-2
3) ацетальдегид
4) этанол
5) этилацетат
Запишите номера выбранных веществ.
- Из предложенного перечня выберите два вещества, с которыми реагирует анилин, но не реагирует бензол.
1) Cu(OH)2
2) Ag2O (NH3/H2O)
3) Br2 (H2O)
4) KOH (H2O)
5) K2Cr2O7 (H2SO4/H2O)
Запишите номера выбранных веществ.
- Установите соответствие между веществом и продуктом, который преимущественно образуется при его взаимодействии с водой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВЕЩЕСТВО | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ С ВОДОЙ |
| А) бутин-1 | 1) фенол |
| Б) циклогексен | 2) 1-хлорбутанол-2 |
| В) бутен-1 | 3) бутанол-2 |
| Г) 1-хлорбутен-2 | 4) бутанон |
| 5) циклогексанол | |
| 6) 4-хлорбутанол-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между схемой превращения веществ и названием реакции, которая лежит в основе этого превращения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА ПРЕВРАЩЕНИЙ | НАЗВАНИЕ РЕАКЦИИ |
| А) глицерин → тристеарин | 1) поликонденсация |
| Б) пропанол-2 → ацетон | 2) этерификация |
| В) метанол→ диметиловый эфир | 3) гидролиз |
| Г) 1,1,1-трихлорэтан → уксусная кислота | 4) дегидрирование |
| 5) внутримолекулярная дегидратация | |
| 6) межмолекулярная дегидратация |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана схема превращений веществ:
![]() Определите, какие из указанных веществ являются веществами Х и Y.
Определите, какие из указанных веществ являются веществами Х и Y.
1) CsOH
2) CsCl
3) H2O
4) Cs
5) CH3OH
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня типов реакций выберите некаталитические.
1) хлорирование этана
2) бромирование бензола
3) гидратация этина
4) окисление этена водным раствором перманганата калия
5) гидролиз карбида алюминия
Запишите номера выбранных ответов.
- Из предложенного перечня выберите все внешние воздействия, которые приведут к увеличению скорости химической реакции жидкой ртути с серой.
1) понижение давления
2) повышение давления
3) увеличение степени измельчения серы
4) добавление катализатора
5) нагревание
Запишите номера выбранных ответов.
- Установите соответствие между названием элемента и характерными степенями окисления, которые он может проявлять в соединениях: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ЭЛЕМЕНТА | СТЕПЕНИ ОКИСЛЕНИЯ |
| А) кислород | 1) -2, -1, 0, +2, +6 |
| Б) азот | 2) 0, +2, +3, +6 |
| В) хлор | 3) -2, -1, 0, +2 |
| 4) -1, 0, +1, +3, +5, +7
5) -3, -2, 0, +1, +2, +3, +4, +5 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой вещества и продуктами, образующемся на инертных электродах при электролизе водного раствора этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
| 1) CH3COOK | 1) O2, H2 |
| 2) NaOH | 2) C2H6, CO2, H2 |
| 3) Mg(NO3)2 | 3) O2, Mg |
| 4) CuBr2 | 4) CH4, CO2, H2 |
| 5) Br2, Cu | |
| 6) MgO, NO2, O2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой соли и средой её водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
| А) AlCl3 | 1) нейтральная |
| Б) K2CO3 | 2) кислая |
| В) KMnO4 | 3) щелочная |
| Г) Na3AsO4 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между способом воздействия на равновесную систему
2NO (г) + Cl2 (г) ↔ 2NOCl (г) + Q,
и направлением смещения химического равновесия при этом воздействии: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) повышение давления | 1) в сторону прямой реакции |
| Б) понижение температуры | 2) в сторону обратной реакции |
| В) повышение концентрации NO | 3) практически не смещается |
| Г) уменьшение концентрации Cl2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между парой веществ и реагентом, с помощью которого можно различить эти вещества (сильные электролиты представлены водными растворами): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ПАРА ВЕЩЕСТВ | РЕАГЕНТ |
| А) NaCl и LiCl | 1) HgS |
| Б) KF и K2CO3 | 2) H2O2 |
| В) Fe(OH)2 и Fe(OH)3 | 3) AgNO3 |
| Г) Mg(NO3)2 и ZnSO4 | 4) Na3PO4 |
| 5) BaBr2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между смесью и методом разделения её на индивидуальные компоненты: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СМЕСЬ | МЕТОД РАЗДЕЛЕНИЯ |
| А) вода и бензол | 1) дистилляция |
| Б) ацетон и вода | 2) выпаривание |
| В) этанол и железо | 3) делительная воронка |
| 4) фильтрование |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответом к заданиям 27–29 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Затем перенесите это число в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Единицы измерения физических величин в бланке ответа указывать не нужно.
- Вычислите массу (в граммах) медного купороса, который образуется при осторожном выпаривании 40 г 20%-го раствора сульфата меди (II). (Запишите число с точность до десятых.)
- В результате полного окисления алюминия кислородом воздуха, в соответствии с термохимическим уравнением 4Al(тв) + 3O2(г) = 2Al2O3(тв) + 2535 кДж, получен оксид алюминия массой 51 г . Вычислите количество теплоты (в кДж), которая выделилось при этом. (Запишите число с точностью до сотых.)
- В результате взаимодействия избытка бензола с бромом в присутствии солей трёхвалентного железа был получен бромоводород количеством 1,2 моль. Укажите массу (в граммах) основного органического продукта. (Запишите число с точностью до десятых.)
Не забудьте перенести все ответы в бланк ответов №1 в соответствии с инструкцией по выполнению работы.
Проверьте, чтобы каждый ответ был записан в строке с номером соответствующего задания.
Часть 2
Для записи ответов на задания 30–35 используйте БЛАНК ОТВЕТОВ № 2. Запишите сначала номер задания (30, 31 и т.д.), а затем его подробное решение. Ответы записывайте чётко и разборчиво.
Для выполнения заданий 30, 31 используйте следующий перечень веществ: сульфид калия, кислород, оксид меди (II), хлорид железа (III), ортофосфорная кислота, гидроксид натрия. Допустимо использование водных растворов веществ.
- Из предложенного перечня выберите два вещества, между которыми возможна окислительно-восстановительная реакция, протекающая при сплавлении, причём выделения газа не наблюдается. При помещении продуктов этой реакции в воду одно из веществ оседает на дно, другое растворяется, а третье всплывает на поверхность. В ответе запишите уравнение только реакции с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
- Из предложенного перечня выберите вещества, между которыми протекает реакция ионного обмена, приводящая к образованию газа. Запишите молекулярное, полное, сокращённое ионное уравнения реакции с участием выбранных веществ.
- Расвтор сульфата хрома (III) по каплям добавляли к избытку раствора гидроксида натрия. Через образовавшийся прозрачный раствор пропускали избыток углекислого газа. В результате этого образовался осадок, который отделили, промыли, высушили и прокалили до постоянной массы. К твёрдому остатку после прокаливания добавили твёрдые нитрат калия и карбонат натрия и снова прокалили. В результате это произошло выделение бесцветного газа без запаха и не поддерживающего горение. Напишите уравнения четырёх описанных реакций.
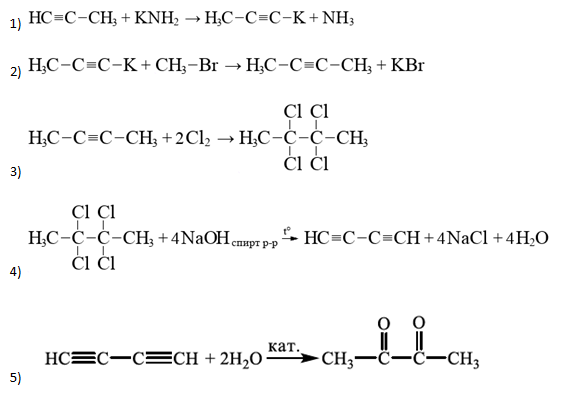
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
![]() При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
- Имеется смесь оксида кобальта (II), оксида кобальта (III) и оксида кобальта (II, III), содержащая примеси оксидов кобольта нестехиометрического состава. Эту смесь массой 0,782 г полностью восстановили водородом, в результате чего было получено твёрдое вещество массой 0,590 г. Эту же смесь массой 1,564 г полностью растворили в растворе бромоводородной кислоты массой 48,6 г с массовой долей растворённого вещества 10%. Рассчитайте максимальную массу кобальта, которую можно ещё растворить в полученном растворе, чтобы в нём содержалась только одна соль.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
- Устойчивое органическое соединение количеством 0,25 моль окислили водным раствором перманганата натрия. В результате образовались только карбонат натрия массой 8,798 г, гидрокарбонат натрия массой 14,028 г, оксид марганца (IV) массой 28,971 г и вода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу неизвестного органического вещества;
2) составьте структурную формулу неизвестного органического вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции описанное в условии задачи (используйте структурные формулы органических веществ).
Ответы:
Первая часть:
- 12
- 543
- 34
- 25
- 321
- 15
- 23
- 3521
- 1264
- 13
- 214
- 15
- 35
- 34
- 35
- 4536
- 2463
- 34
- 145
- 345
- 354
- 2115
- 2313
- 1112
- 4325
- 314
- 12,5
- 633,75
- 188,4
Вторая часть:
- 3K2S + 2FeCl3 = 2FeS + S + 6KCl
S-2 – 2e = S0 1
Fe+3 + 1e = Fe+2 2
Сера в степени окисления -2 (или K2S) является восстановителем.
Железо в степени окисления +3 (или FeCl3) является окислителем.
- 2H3PO4 + 3K2S = 2K3PO4 + 3H2S
2H3PO4 + 6K+ + 3S2- = 6K+ + 2PO43- + 3H2S
2H3PO4 + 3S2- = 2PO43- + 3H2S
- 1) 12NaOH + Cr2(SO4)3 = 2Na3[Cr(OH)6] + 3Na2SO4
2) Na3[Cr(OH)3] + 3CO2 = Cr(OH)3↓ + 3NaHCO3
3) 2Cr(OH)3 = Cr2O3 + 3H2O
4) Cr2O3 + 3KNO3 + 2Na2CO3 = 2Na2CrO4 + 3KNO2 + 2CO2↑
- 590 мг
Видео-объяснение смотрите на Ютуб по ссылке или ниже
- CH2O — формальдегид
Видео-объяснение смотрите на Ютуб по ссылке или ниже
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ всех лет (реальные, пробные и тренировочные задания) вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку

Вариант содержит огромное количество ошибок!Закидать помидорами составителя!!!
Здравствуйте. Любой вариант любого составителя может содержать описки/ошибки. Для этого и существуют комментарии, чтобы можно было об этом сказать и их исправить — это называется обратная связь. Если вам мои варианты кажутся плохими, просьба просто НЕ пользоваться сайтом. А если нет, то я готов к конструктивному и взаимоуважительному диалогу.
Извините, пожалуйста, а в 22 случайно нет ошибки? Мне кажется правильный ответ 2115. При электролизе нитрата магния образуется водород и кислород, там не будет магния
Здравствуйте. Конечно, это опечатка в ответе. Спасибо за внимательность. Исправим!
А в 9 задании точно ответ 1254? Мне кажется, 1264. При взаимодействии серной кислоты на хромат натрия образуется бихромат.
Заранее спасибо!
Извините, пожалуйста, а в 22 случайно нет ошибки? Мне кажется правильный ответ 2115. При электролизе нитрата магния образуется водород и кислород, там не будет магния
В 9 правильный ответ 1264. При взаимодействии кислоты на хроматы образуются бихроматы
Вы правы!
«Смущают» ответы на задания №9 (3 вопрос) и №22 (3 вопрос) в пробном варианте 9
Спасибо за внимательность! Поправил.
Пробный вариант № 9: вопрос 22 -при электролизе раствора нитрата магния на катоде выделится водород, а не магний
вопрос 25: Fe(OH)2 и Fe(OH)3 — не растворы!
Fe(OH)2 и Fe(OH)3 — это очень слабые электролиты. И абсолютно не растворимых оснований не бывает, поэтому в рамках этого задания это не являлось нарушением. Но чтобы убрать сомнения, я поправил формулировку.
В 32 задании вторая реакция немного не корректная.
Можно вопрос? В четвертой реакции 32 задания, получится не NaCrO2? или он окислится?
Здравствуйте. Спасибо, поправил опечатку во втором уравнении.
А в чётвёртом уравнении, действительно, происходит окисление хрома, поэтому получается Na2CrO4
Задача 34 полностью притянута за уши для решения авторским способом. Настоящая и адекватная задача решается несколькими способами, однако здесь мы можем наблюдать невозможность ее решения через систему уравнений для нахождения количества веществ в смеси, потому что числа взяты с дуба.
Здравствуйте. Спасибо за «жёсткий комментарий». Числа действительно в задачи вымышленные. Цель была показать как решать задачи через закон сохранения массы веществ и так называемую «атомистику», а не через систему.