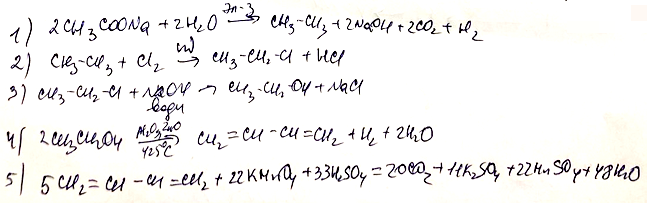Скачать Пробный вариант 9. ЕГЭ 2020 по химии с ответами в формате pdf
Вариант 9
Для выполнения заданий 1 – 3 используйте следующий ряд химических элементов:
1) Cl; 2) Br; 3) S; 4) Se; 5) V.
Ответом в заданиях 1 – 3 является последовательность цифр, под которыми указаны химические элементы в данном ряду
- Определите, атомам каких из указанных в ряду элементов в основном состоянии не хватает двух электронов для завершения внешнего электронного слоя. Запишите в поле ответа номера выбранных элементов.
- Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одном периоде. Расположите выбранные элементы в порядке увеличения суммарного числа всех элементарных частиц, в образуемых ими атомах. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
- Из числа указанных в ряду элементов выберите два элемента, которые способны в соединениях проявлять степени окисления +1, +3, +5, +7. Запишите в поле ответа номера выбранных элементов.
- Из предложенного перечня выберите два ряда веществ, в котором они расположены в порядке уменьшения температур кипения.
1) глицерин, этанол, гексан, бутан
2) гексан, бутан, этанол, глицерин
3) бутан, гексан, глицерин, этанол
4) иодоводород, бромоводород, хлороводород, фтороводород
5) фтороводород, иодоводород, бромоводород, хлороводород
Запишите в поле ответа номера выбранных рядов веществ.
- Установите соответствие между формулой кислоты и полным названием этой кислоты: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА КИСЛОТЫ | НАЗВАНИЕ |
| А) HPO3 | 1) ортофосфорная |
| Б) H3PO4 | 2) пирофосфорная |
| В) H4P2O7 | 3) метафосфорная |
| 4) фосфорная |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня выберите два вещества, с каждым из которых взаимодействует углерод.
1) P
2) Si
3) HCl
4) Al
5) CO
Запишите в поле ответа номера выбранных веществ.
- В одну из пробирок с раствором гидрокарбоната кальция добавили раствор сильного электролита Х, а в другую – раствор сильного электролита Y. В результате в первой пробирке наблюдали образование осадка, а во второй – выделение газа. Из предложенного перечня выберите вещества Х и Y, которые могут вступать в описанные реакции.
1) хлорная кислота
2) гидросульфит натрия
3) сернистая кислота
4) гидроксид натрия
5) гидроксид цинка
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
- Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) Na2SO4 | 1) HCl, NaHCO3, O2 |
| Б) H2 | 2) KOH, O2, Sr(OH)2 |
| В) SO2 | 3) Sr(OH)2, HNO3, HBr |
| Г) Sn(OH)2 | 4) CuO, N2, S |
| 5) Ba(NO3)2, (CH3COO)2Pb, SrBr2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами, которые образуются в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) Na2SO4 и C (t) | 1) Na2CO3 |
| Б) Na2O2 и CO2 | 2) Na2CO3, O2 |
| В) Na2O и CO2 | 3) Na2CO3, SO2 |
| Г) NaOH и CO2 (изб.) | 4) Na2S, CO |
| 5) Na2CO3, H2O | |
| 6) NaHCO3 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1) сульфат стронция
2) хлорид калия
3) гипохлорит натрия
4) хлорат натрия
5) перхлорат натрия
Запишите в таблицу номера веществ под соответствующими буквами.
- Установите соответствие между классом/группой органических соединений и формулой его представителя: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| КЛАСС/ГРУППА
ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ |
ФОРМУЛА ВЕЩЕСТВА |
| А) алкины
Б) алкадиены В) эфиры |
1) C4H6
2) C2H4 3) HCOOCH3 4) CH3COOH |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня выберите два верных утверждения о феноле.
1) атом кислорода в молекуле образует одну сигма-связь и две пи-связи
2) атом кислорода в молекуле образует две сигма-связи и одну пи-связь
3) атом кислорода в молекуле образует две сигма-связи
4) атомные орбитали атомов углерода находятся в состоянии sp2-гибридизации
5) атомные орбитали атомов углерода находятся в состоянии sp3-гибридизации
Запишите в поле ответа номера выбранных утверждений.
- Из предложенного перечня выберите два вещества, при гидратации каждого из которых образуется одноатомный спирт.
1) бутен-2
2) пропин
3) 1,1-дихлорбутан
4) метилпропен
5) хлорбензол
Запишите в поле ответов номера выбранных веществ.
- Из предложенного перечня выберите два вещества, с которыми реагирует муравьиная кислота.
1) C2H5OH
2) C6H5CH3
3) CH2(OH) – CH2(OH)
4) C6H6
5) CH3COOH
Запишите в поле ответа номера выбранных веществ.
- Из предложенного перечня выберите два вещества, с которыми реагирует аминоуксусная кислота.
1) серин
2) кумол
3) метиламин
4) пропилформиат
5) дивинил
Запишите в поле ответа номера выбранных веществ.
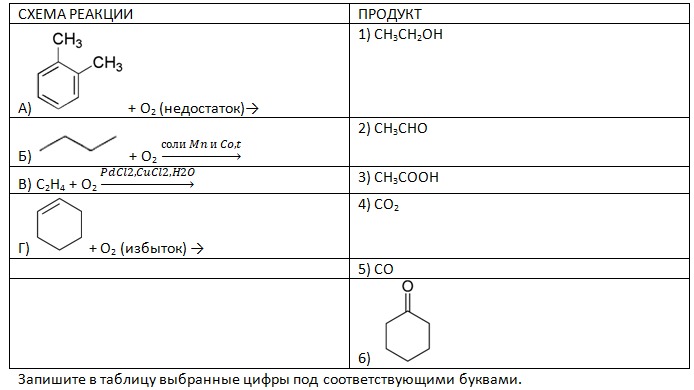
- Установите соответствие между схемой реакции и углеродсодержащим продуктом, который преимущественно образуется в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
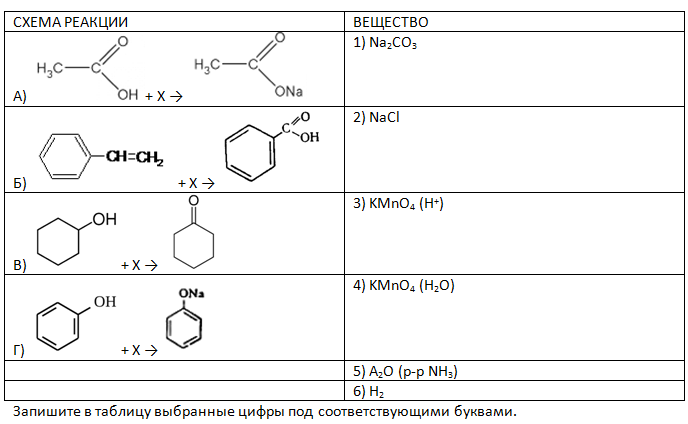
- Установите соответствие между схемой реакции и веществом Х, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1) CH3NO2
2) CH3COONH4
3) CH3C(O)ONHCH3
4) CH3C(O)NHCH3
5) CH3NH2
Запишите в таблицу номера веществ под соответствующими буквами.
- Из предложенного перечня типов реакций выберите два типа реакций, к которым можно отнести электролиз водного раствора сульфата меди (II).
1) окислительно-восстановительная
2) необратимая
3) каталитическая
4) соединения
5) поликонденсация
Запишите в поле ответа номера выбранных типов реакций.
- Из предложенного перечня выберите два внешних воздействия/фактора, которые НЕ влияют на скорость реакции разложения аммиака на простые веществ.
1) концентрация аммиака
2) давление
3) температура
4) концентрация водорода
5) концентрация азота
Запишите в поле ответа номера выбранных внешних воздействий/факторов.
- Установите соответствие между формулой уравнением реакции и формулой вещества, являющегося восстановителем в данной реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | ВОССТАНОВИТЕЛЬ |
| А) NO + NO2 + 2NaOH = 2NaNO2 + H2O | 1) NO2 |
| Б) SeO2 + 2H2Se = 3Se + 2H2O | 2) H2Se |
| В) Cl2 + SeO2 + 2H2O = 2HCl + H2SeO4 | 3) Cl2 |
| 4) SeO2 | |
| 5) NO |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой соли и продуктом электролиза водного раствора этой соли, который образовался на катоде (электроды инертные): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ПРОДУКТ НА КАТОДЕ |
| А) AgNO3 | 1) водород |
| Б) BaCl2 | 2) кислород |
| В) Na2SO4 | 3) металл |
| Г) CuSO4 | 4) галоген |
| 5) оксид серы (IV) | |
| 6) оксид азота (IV) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой соли и отношением этой соли к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
| А) NaF | 1) гидролизуется по катиону |
| Б) CuSO4 | 2) гидролизуется по аниону |
| В) (CH3COO)3Al | 3) гидролизу не подвергается |
| Г) Rb3PO4 | 4) гидролизуется по катиону и аниону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между уравнением обратимой реакции и направлением смещения химического равновесия при повышении температуры: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) С (тв) + H2O (г) ↔ CO (г) + H2 (г) – Q | 1) смещается в сторону прямой реакции |
| Б) Fe2О3(тв) + 3H2(г) ↔ 2Fe(тв) + 3H2O(г) – Q | 2) смещается в сторону обратной реакции |
| В) CO(г) + 2H2(г) ↔ CH3OH(г) + Q | 3) практически не смещается |
| Г) CO2(г) + С(тв) ↔ 2СО(г) — Q |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между двумя веществами, и реактивом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВЕЩЕСТВА | РЕАКТИВ |
| А) бензол и стирол | 1) NaOH/H2O |
| Б) фенол (водн. р-р) и бензол | 2) Cu(OH)2, 20C |
| В) сахароза и лактоза | 3) KMnO4/H2O |
| Г) этанол и пропандиол-1,2 | 4) FeCl3 |
| 5) Cu(OH)2, t |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между веществом и основной областью его применения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВЕЩЕСТВО | ОБЛАСТЬ ПРИМЕНЕНИЯ |
| А) OF2 | 1) окислитель ракетного топлива |
| Б) Na3AlF6 | 2) при получении алюминия |
| В) Р (красный) | 3) для производства спичек |
| 4) для обеззараживания воды |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Вычислите массу Zn(NO3)2∙6H2O (в граммах), который необходим для приготовления 750 г 12,6%-го раствора нитрата цинка. (Запишите число с точностью до десятых.)
- Какой объём водорода (в литрах) потребуется для получения метанола по реакции с угарным газом объёмом 4 л? Объёмы газов измерены в одинаковых условиях, метанол в условиях опыта — газ. (Запишите число с точностью до целых.)
- Вычислите объём газа (в литрах), который выделился при взаимодействии сульфида натрия массой 78 г с избытком соляной кислоты. (Запишите число с точностью до целых.)
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
нитрат серебра (I), водород, хлорид калия, бромид калия, сульфат свинца (II), фосфин. Допустимо использование водных растворов веществ.
- Из предложенного перечня веществ выберите вещества, между которыми окислительно-восстановительная реакция протекает с образованием металла. Выделение газа в ходе этой реакции не наблюдается. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
- Из предложенного перечня веществ выберите два вещества, которые вступают в реакцию ионного обмена с образованием жёлтого осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
- Фосфор сожгли в избытке хлора, образующееся твёрдое вещество смешали с фосфором и нагрели. Продукт реакции обработали небольшим количеством воды, при этом выделился бесцветный газ с резким запахом. Раствор добавили к подкисленному серной кислотой раствору перманганата калия, который в результате реакции обесцветился и образовался осадок. Напишите уравнения четырёх описанных реакций.
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
При написании уравнений реакций используйте структурные формулы органических веществ.
- Смесь порошков магния и цинка общей массой 8,9 г разделили на две равные части. Одну часть полностью сожгли в избытке кислорода и получили 6,05 г продуктов сгорания. При добавлении 40 г 10%-ного раствора гидроксида натрия происходит растворение одного из продуктов. Вторую часть смеси полностью сожгли на воздухе и получили 5,85 г продуктов сгорания. При добавлении воды к продуктам сгорания второй части смеси выделяется газ с резким запахом, который широко применяется в химической промышленности. Вычислите объём (в л, н.у.) этого газа. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических венличин).
- В состав вещества входят атомы углерода, водорода и азота, причём массовая доля атомов углерода в нём 53,33%. Масса азота, полученного из 0,546 г вещества, равна 0,170 г. Относительная плотность этого вещества по озону равна 0,9375. Известно, что данное вещество реагирует раствором нитрита калия в присутствиии соляной кислоты с образованием органического вещества, относящегося к другому классу, и выделением газа, входящего в состав атмосферы.
На основании данных условия задания:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции этого вещества с раствором нитрита калия в присутствии соляной кислоты (используйте структурные формулы органических веществ).
Система оценивания экзаменационной работы по химии
Часть 1
За правильный ответ на каждое из заданий 1–6, 11–15, 19–21, 26–29 ставится 1 балл.
Задание считается выполненным верно, если экзаменуемый дал правильный ответ в виде последовательности цифр или числа с заданной степенью точности.
Задания 7–10, 16–18, 22–25 считаются выполненными верно, если правильно указана последовательность цифр.
За полный правильный ответ заданий 7–10, 16–18, 22–25 ставится 2 балла; если допущена одна ошибка – 1 балл; за неверный ответ (более одной ошибки) или его отсутствие – 0 баллов.
| Номер задания | Правильный ответ |
| 1 | 34 |
| 2 | 542 |
| 3 | 12 |
| 4 | 15 |
| 5 | 312 |
| 6 | 24 |
| 7 | 41 |
| 8 | 5423 |
| 9 | 4216 |
| 10 | 23 |
| 11 | 113 |
| 12 | 34 |
| 13 | 14 |
| 14 | 13 |
| 15 | 13 |
| 16 | 5324 |
| 17 | 1331 |
| 18 | 54 |
| 19 | 12 |
| 20 | 45 |
| 21 | 524 |
| 22 | 3113 |
| 23 | 2142 |
| 24 | 1121 |
| 25 | 3452 |
| 26 | 123 |
| 27 | 148,5 |
| 28 | 8 |
| 29 | 22 |
Часть 2
Критерии оценивания заданий с развёрнутым ответом
За выполнение заданий 30, 31 ставится от 0 до 2 баллов; задания 35 – от 0 до 3 баллов; заданий 32 и 34 – от 0 до 4 баллов; задания 33 – от 0 до 5 баллов.
Задание 30
Вариант ответа:
PH3 + 8AgNO3 + 4H2O → 8Ag + H3PO4 + 8HNO3
8 Ag+1 + ē → Ag0
1 P-3 – 8ē → P+5
Фосфин или фосфор в степени окисления -3 является восстановителем.
Нитрат серебра (I) или серебро в степени окисления +1 – окислителем
Задание 31
Вариант ответа:
AgNO3 + KBr = AgBr + KNO3
Ag+ + NO3— + K+ + Br— = AgBr + K+ + NO3—
Ag+ + Br— = AgBr
Задание 32
Вариант ответа:
2P + 5Cl2 = 2PCl5
3PCl5 + 2P = 5PCl3
PCl3 + 3H2O = H3PO3 + 3HCl↑
15H3PO3 + 6KMnO4 + 3H2SO4 = 11H3PO4 + 3K2SO4 + 2Mn3(PO4)2↓ + 9H2O
Задание 33
Примечание. Допустимо использование структурных формул разного вида (развёрнутой, сокращённой, скелетной), однозначно отражающих порядок связи атомов и взаимное расположение заместителей и функциональных групп в молекуле органического вещества.
Задание 34
Объяснение этой задачи вы можете найти на Ютуб по ссылке
Ответ: 0,448 л
Задание 35
M (CxHyNz) = M (O3) ∙ DO3 (CxHyNz) = 48 г/моль ∙ 09375 = 45 г/моль
n (CxHyNz) = 0546 г/45 г/моль = 0,012 моль
n (N2) = 0,170 г/28 г/моль = 0,006 моль
n (N) = 2 ∙ n (N2) = 2 ∙ 0,006 моль = 0,012 моль
0,012 моль вещества содержат 0,012 моль N, следовательно 1 моль вещества содержит 1 моль N, т.е. в формуле 1 атом азота.
m (C) = Mr (CxHyNz) ∙ w (CxHyNz) = 45 ∙ 0,5333 = 24 (г)
n (С) = 24 г/12 г/моль = 2 моль.
Следовательно 1 моль вещества содержит 2 моль углерода, т.е. в формуле 2 атома углерода.
N (H) = (M (CxHyNz) – M (C2N)) /1 г/моль = (45 г/моль – 38 г/моль) /1 г/моль = 7
Следовательно, молекулярная формула C2H7N
Азотсодержащим веществом может быть либо амин либо нитросоединения. Предполагаем, что исходное вещество амин. Так как вещество реагирует с азотистой кислотой (нитрит калия + соляная кислота), то оно относится к первичным аминам, потому что вторичные амины в эту реакцию не вступают, равно как и нитросоединения.
Структурная формула CH3 – CH2 – NH2
Уравнение реакции:
CH3 – CH2 – NH2 + KNO2 + HCl → CH3 – CH2 – OH + N2 + KCl + H2O
Также вы можете скачать:
- Пробный вариант №1 ЕГЭ 2020 г. (аналог демонстрационного варианта ЕГЭ 2020 г.) с ответами в формате pdf
- Пробный вариант 2. ЕГЭ 2020 по химии с ответами в формате pdf
- Пробный вариант 3. ЕГЭ 2020 по химии с ответами в формате pdf
- Пробный вариант 4. ЕГЭ 2020 по химии с ответами в формате pdf
- Пробный вариант 5. ЕГЭ 2020 по химии с ответами в формате pdf
- Пробный вариант 6. ЕГЭ 2020 по химии с ответами в формате pdf
- Пробный вариант 7. ЕГЭ 2020 по химии с ответами в формате pdf
- Пробный вариант 8. ЕГЭ 2020 по химии с ответами в формате pdf
- Пробный вариант 9. ЕГЭ 2020 по химии с ответами в формате pdf
- Демонстрационный вариант ЕГЭ 2020 (с сайта ФИПИ)
- Кодификатор ЕГЭ 2020 (с сайта ФИПИ)
- Спецификация ЕГЭ 2020 (с сайта ФИПИ)
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ всех лет вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку