Скачать Пробный вариант 7. ЕГЭ 2021 по химии с ответами в формате pdf
Ответы вы найдёте в конце страницы
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
Часть 1
Ответом к заданиям 1–26 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Цифры в ответах на задания 5, 8, 9, 11, 16, 17, 21–26 могут повторяться.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
1) F 2) O 3) Cr 4) Ne 5) Cu
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
- Укажите элементы, которые могут образовывать положительно заряженный ион с зарядом равным номеру группы периодической системы и не имеющий неспаренных электронов в основном состоянии.
Запишите номера выбранных элементов.
- Из указанных в ряду химических элементов выберите три элемента-неметалла, находящихся в одном периоде периодической системы. Расположите выбранные элементы в порядке увеличения массовых чисел их стабильных изотопов .
Запишите номера выбранных элементов в нужной последовательности.
- Из указанных в ряду элементов выберите два элемента, которые не могут проявлять степень окисления равную +2.
Запишите номера выбранных элементов.
- Из предложенного перечня выберите два вещества, структурные единицы которых содержат связи, образующиеся перекрыванием р-орбиталей по обе стороны от линии соединения атомов.
1) H2SO4
2) Cu
3) KCl
4) Na2CO3
5) CH4
Запишите номера выбранных веществ.
- Усоответствие между формулой вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) SiC | 1) гидроксид |
| Б) CaC2 | 2) гидрид |
| В) SrH2 | 3) гидрат |
| 4) карбид | |
| 5) силицид |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня соединений выберите два оксида, которые реагируют с оксидом углерода (IV), но не реагируют с гидроксидом калия.
1) Na2O2
2) OF2
3) Li2O
4) SO2
5) BaO
Запишите номера выбранных веществ.
- В двух пробирках находился раствор гидросульфита аммония. В первую пробирку добавили раствор вещества Х, а во вторую – раствор вещества Y. В результате в первой пробирке образовался белый осадок, во второй – выделился газ, окрашивающий влажную лакмусовую бумажку в красный цвет. Из предложенного перечня выберите вещества Х и Y, которые могут вступить в описанные реакции.
1) гидроксид натрия
2) бромид калия
3) серная кислота
4) аммиак
5) гидроксид бария
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) H2 | 1) CuSO4, CO2, KHCO3 |
| Б) Cl2O7 | 2) NaNO3, SiO2, O2 |
| В) Ba(OH)2 | 3) CuO, N2, Sr |
| Г) Na3PO4 | 4) Na2O, H2O, CsOH |
| 5) AgNO3, CaCl2, LiBr |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами в этой реакции: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) K2S2O3 + HCl (p-p) → | 1) K2SO4 + HCl |
| Б) K2SO3 + HCl (p-p) → | 2) KCl + S + SO2 + H2O |
| В) K2S + HCl (p-p) → | 3) KCl + SO2 + H2O |
| Г) K2SO3 + Cl2 + H2O → | 4) KClO3 + H2S |
| 5) KCl + S | |
| 6) KCl + H2S |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана следующая схема превращений:
 Определите, какие из указанных веществ являются веществами Х и Y.
Определите, какие из указанных веществ являются веществами Х и Y.
1) гидроксид меди (II)
2) гидроксид калия
3) вода
4) хлорид аммония
5) азотная кислота
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
А) 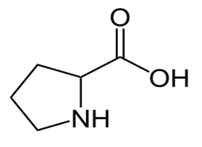 |
1) гомоциклические аминокислоты |
Б) 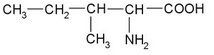 |
2) гетероциклические аминокислоты |
| В) C6H5CH2CH(NH2)COOH | 3) ациклические аминокислоты |
| 4) алициклические аминокислоты |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня выберите два вещества, в составе молекул которых нет первичных атомов углерода.
1) стирол
2) фенол
3) пентен-2
4) этанол
5) циклопентан
Запишите номера выбранных веществ.
- Из предложенного перечня выберите два вещества, которые не вступают в реакции 1,4-присоединения.
1) 2-метилбутадиен-1,3
2) 2-метилпентадиен-1,4
3) гептадиен-1,6
4) бутадиен-1,3
5) 2-хлорбутадиен-1,3
Запишите номера выбранных веществ.
- Из предложенного перечня выберите два вещества, с каждым из которых реагирует пропантриол-1,2,3.
1) Ag
2) CH3OH
3) Cu2O
4) H2
5) HNO3
Запишите номера выбранных веществ.
- Из предложенного перечня выберите два вещества, с помощью которых можно различить аланин и глюкозу.
1) Cu(OH)2, t
2) HNO2
3) H2
4) KOH
5) HBr
Запишите номера выбранных веществ.
- Установите соответствие между дигалогеналканом и продуктом его взаимодействия с избытком спиртового раствора гидроксида калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ДИГАЛОГЕНАЛКАНА | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ СО ЩЁЛОЧЬЮ |
| А) 1,2-дибромпропан | 1) 2-метилпропен |
| Б) 2,3-дихлорбутан | 2) пропин |
| В) 1,2-дибромэтан | 3) этин |
| Г) 1,1-дихлорбутан | 4) бутин-2 |
| 5) бутин-1 | |
| 6) пропен |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
| А) CH3COOH и K2S | 1) пропионат калия |
| Б) HCOOH и KOH | 2) метилат калия |
| В) HCOOH и CuO (t) | 3) формиат меди (II) |
| Г) CH3OH и K | 4) формиат калия |
| 5) ацетат калия | |
| 6) углекислый газ |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана схема превращений веществ:
 Определите, какие из указанных веществ являются веществами Х и Y.
Определите, какие из указанных веществ являются веществами Х и Y.
1) Br2/FeBr3
2) C2H6/t
3) Br2/свет
4) C2H5Br/AlCl3, t
5) HBr/H2O
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня типов реакций выберите те, к которым можно отнести реакцию между раствором гидроксида бария и метилпропионатом.
1) реакция щелочного гидролиза
2) необратимая
3) обратимая
4) реакция разложения
5) окислительно-восстановительная
Запишите номера выбранных ответов.
- Из предложенного перечня выберите все воздействия, которые увеличивают скорость реакции обжига сульфида малоактивного металла на воздухе:
1) повышение температуры
2) использование чистого кислорода вместо воздуха
3) измельчение сульфидной руды
4) добавление ингибитора
5) понижение общего давления
Запишите номера выбранных ответов.
- Установите соответствие между схемой реакции и свойством, которое проявляет азот в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | СВОЙСТВО АЗОТА |
| А) NO2 + KOH → KNO2 + KNO3 + H2O | 1) является окислителем |
| Б) S + HNO3 → SO2 + NO2 + H2O | 2) является восстановителем |
| В) CuO + HNO3 → Cu(NO3)2 + H2O | 3) является и окислителем, и восстановителем |
| 4) не проявляет окислительно-восстановительных свойств |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой соли и продуктом, образующемся на инертном катоде при электролизе водного раствора этой соли: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ПРОДУКТ(-Ы) НА КАТОДЕ |
| 1) Mg(NO3)2 | 1) металл |
| 2) NiSO4 | 2) кислород |
| 3) CuCl2 | 3) сернистый газ |
| 4) K2SO4 | 4) металл, водород |
| 5) водород | |
| 6) оксид азота (II) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием соли и её отношением к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
| А) карбонат аммония | 1) гидролиз не протекает |
| Б) карбонат цезия | 2) гидролиз по катиону |
| В) сульфид хрома (III) | 3) гидролиз по аниону |
| Г) фосфат натрия | 4) гидролиз по катиону и аниону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между способом воздействия на равновесную систему
ClO2 (г) + H2O (ж) ↔ H+ (p-p) + ClO3— (p-p) + HClO2 (p-p) + Q,
и направлением смещения химического равновесия при этом воздействии: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) повышение давления | 1) вправо |
| Б) понижение температуры | 2) влево |
| В) добавление твёрдого хлората калия | 3) практически не смещается |
| Г) добавление соляной кислоты |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между парой веществ и реагентом, с помощью которого можно обнаружить водный раствор каждого вещества пары: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ПАРА ВЕЩЕСТВ | РЕАГЕНТ |
| А) Ba(NO3)2 и K2SiO3 | 1) KF |
| Б) Cu(NO3)2 и Fe(NO3)3 | 2) H2SO4 |
| В) AlCl3 и NaBr | 3) AgNO3 |
| Г) Mg(NO3)2 и HCOONH4 | 4) LiOH |
| 5) BaCl2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между мономером и продуктом его полимеризации: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| МОНОМЕР | ПОЛИМЕР |
| А) стирол | 1) (–CH2–CH2–)n |
| Б) пропилен | 2) (–CH2–CH(C6H5)–)n |
| В) изопрен | 3) (–CH2–CH(CH3)–)n |
| 4) (–CH2–C(СН3)=CH–CH2–)n |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответом к заданиям 27–29 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Затем перенесите это число в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Единицы измерения физических величин в бланке ответа указывать не нужно.
- Вычислите массовую долю (%) серной кислоты в растворе, образующемся при смешении 120 г 20%-ного раствора серной кислоты с 40 г 50%-ного раствора бромоводородной кислоты (Запишите число с точность до целых.)
- После полного сжигания метиламина в необходимом количестве кислорода и приведения к нормальным условиям образовалась газовая смесь объёмом 6,72 л. Рассчитайте объём кислорода (в литрах), затраченного на сгорание метиламина. (Запишите число с точностью до сотых.)
- Вычислите массу алюминия (в граммах), необходимого для полного вытеснения меди из её двухвалентного хлорида массой 81 г (Запишите число с точностью до десятых.)
Не забудьте перенести все ответы в бланк ответов №1 в соответствии с инструкцией по выполнению работы.
Проверьте, чтобы каждый ответ был записан в строке с номером соответствующего задания.
Часть 2
Для записи ответов на задания 30–35 используйте БЛАНК ОТВЕТОВ № 2. Запишите сначала номер задания (30, 31 и т.д.), а затем его подробное решение. Ответы записывайте чётко и разборчиво.
Для выполнения заданий 30, 31 используйте следующий перечень веществ: гидрокарбонат калия, хлорат калия, гидросульфит натрия, соляная кислота, сероводород, перманганат калия. Допустимо использование водных растворов веществ.
- Из предложенного перечня выберите вещества, между которыми возможна окислительно-восстановительная реакция, приводящая к образованию двух солей и выделению бесцветного газа с резким запахом. В ответе запишите уравнение только реакции с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
- Из предложенного перечня выберите два вещества, между которыми протекает реакция ионного обмена, приводящая к выделению газа без цвета и запаха. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
- Гематит сплавили с гидроксидом натрия. Твёрдый продукт реакции растворили в стехиометрическом количестве азотной кислоты. Затем в образовавшийся раствор на некоторое время опустили медную проволоку, в результате чего изменилась окраска раствора. Далее из полученного раствора выделили не содержащий медь продукт, высушили и прокалили до постоянной массы, в результате чего выделился газ бурого цвета. Напишите уравнения четырёх описанных реакций.
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
![]() При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
- Смесь оксида железа (II), оксида железа (III) и оксида железа (II, III) общей массой 161 г полностью восстановили углеродом. При этом образовалось только железо и углекислый газ объёмом 39,2 л. Образовавшийся порошок железа засыпали в раствор хлорида меди (II) массой 1200 г с массовой долей соли 25% и оставили на несколько дней. Рассчитайте массовую долю (%) хлорида меди (II) в конечном растворе, считая, что железо прореагировало полностью, а в исходной смеси оксидов железа могли содержаться примеси оксидов железа нестехиометрического состава.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
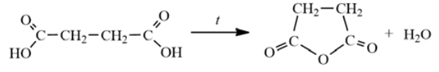
- Вещество А содержит 48% углерода, 4% водорода и 48% кислорода по массе. Известно, что вещество А относится к гетероциклическим соединениям и получается дегидратацией при нагревании вещества Б, которое не содержит третичных и четвертичных атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А путём дегидратации вещества Б при нагревании (используйте структурные формулы органических веществ).
Ответы:
Первая часть:
- 35
- 214
- 14
- 14
- 442
- 35
- 53
- 3415
- 2361
- 52
- 231
- 25
- 23
- 25
- 12
- 2435
- 5432
- 41
- 12
- 123
- 314
- 5415
- 4343
- 1122
- 2434
- 234
- 15
- 10,08
- 10,8
Вторая часть:
- 6NaHSO3 + KClO3 = KCl + 3Na2SO4 + 3SO2↑ + 3H2O
S+4 – 2e = S+6 3
Cl+5 + 6e = Cl-1 1
Сера в степени окисления +4 (или NaHSO3) является восстановителем.
Хлор в степени окисления +5 (или KClO3) является окислителем.
- KHCO3 + HCl = KCl + H2O + CO2↑
K+ + HCO3— + H+ + Cl— = K+ + Cl— + H2O + CO2↑
HCO3— + H+ = H2O + CO2↑
- 1) Fe2O3 + 2NaOH = 2NaFeO2 + H2O
2) NaFeO2 + 4HNO3 = NaNO3 + Fe(NO3)3 + 2H2O
3) 2Fe(NO3)3 + Cu = 2Fe(NO3)2 + Cu(NO3)2
4) 4Fe(NO3)2 = 2Fe2O3 + 8NO2 + O2
- 4%
Видео-объяснение смотрите на Ютуб по ссылке или ниже
- Общая формула вещества А – CxHyOz
x : y : z = 48/12 : 4/1 : 48/16 = 4 : 4 : 3. Следовательно, молекулярная формула С4Н4О3.
- Соединение С4Н4О3 является гетероциклическим, а значит в состав цикла входят не только атому углерода, но и атомы кислорода. Учитывая, что это вещество образуется путём дегидратации, то можно предположить, что вещество А получается из карбоновой кислоты, так как при дегидратации спиртов образуются алкены, а альдегиды и простейшие эфиры не подвергаются дегидратации . Но так как образуется цикл, то в веществе Б должно быть две карбоксильные группы. И так как по условию задачи сказано, что вещество Б не содержит третичные и четвертичные атомы углерода, то значит его цепочка прямая и неразветвлённая, а значит карбоксильные группы расположены по концам. Как следствие, будет образовываться пятичленный цикл вещества А.
Структурная формула вещества А: 
- 3. Уравнение реакции:
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ всех лет (реальные, пробные и тренировочные задания) вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку


в 27 разве ответ не 27,5% ?
Здравствуйте, нет, ответ 15%. Вы, наверное, не заметили, что в условии задачи смешивали растворы разных кислот, которые не реагируют между собой. Поэтому сколько H2SO4 было в исходном растворе, столько и осталось в конечном. Значит в исходном растворе было H2SO4 120*0,2 = 24 г. Масса конечного раствора слагается из масс двух смешиваемых растворов, то есть 120 + 40 = 160 г. Следовательно массовая доля H2SO4 в конечном растворе равна 24/160 = 0,15 или 15%
Добрый вечер, почему в номере 14 у нас ответ получается 25? Он у меня получился методом исключения. Поэтому интересно каким образом многоатомный спирт пропантриол-1,2,3 будет реагировать CH3OH?
Здравствуйте. Спирты могут реагировать друг с другом с образованием простых эфиров. Поэтому с пропантриолом-1,2,3 будет образовываться вещество CH2(OCH3)CH(OCH3)CH2(OCH3) — триметиловый эфир глицерина
Здравствуйте. Можете, пожалуйста, пояснить 32 задание ( 4 — ая реакция). Перед нами разложение нитрата железа (2). А почему же в продуктах реакции степень окисления с +2 перескочила до +3 и мы не взяли в качестве оксида ( FeO)
Здравствуйте. Это исключение, которое обязательно надо запомнить! Нитрат железа двухвалентного разлагается именно с образованием оксида железа трёхвалентного