Скачать Пробный вариант 5. ЕГЭ 2021 по химии с ответами в формате pdf
Часть 1
Ответом к заданиям 1–26 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Цифры в ответах на задания 5, 8, 9, 11, 16, 17, 21–26 могут повторяться.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду
1) F 2) Cr 3) Mn 4) O 5) P
- Определите , атомы каких из указанных в ряду элементов в основном состоянии содержат валентные электроны на разных энергетических уровнях.
Запишите в поле ответа номера выбранных элементов.
- Из указанных в ряду химических элементов выберите три элемента-неметалла. Расположите выбранные элементы в порядке увеличения численного значения отношения количества нейтронов к количеству протонов в их атомах. Запишите в поле ответа номера выбранных элементов.
- Из числа указанных в ряду элементов выберите два элемента, которые не могут проявлять валентность и степень окисления равную номеру группы, в которой они расположены.
Запишите в поле ответа номера выбранных элементов.
- Из предложенного перечня выберите два вещества немолекулярного строения, которые очень тугоплавки, обладают высокой прочностью и твёрдостью.
1) карборунд
2) формиат кальция
3) этилен
4) алмаз
5) фосфорная кислота
Запишите в поле ответа номера выбранных веществ.
- Усоответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) ляпис | 1) оксид |
| Б) цианид калия | 2) основание |
| В) угарный газ | 3) соль средняя |
| 4) соль основная |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня соединений выберите два соединения, которые в водном растворе вступают в реакцию с хлором.
1) NaClO4
2) O2
3) HF
4) FeCl2
5) K2SO3
Запишите в поле ответа номера выбранных веществ.
- Имеется две пробирки с раствором гидроксида бария. К одной из пробирок добавили раствор соли Х, а через другую пропустили газ Y. В результате в первой пробирке наблюдалось выпадение цветного осадка, а во второй – белого. Из предложенного перечня выберите вещества Х и Y, которые могут вступить в описанные реакции.
1) MgCl2
2) NH3
3) Fe(NO3)3
4) SO2
5) KHSO3
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) K2SO3 | 1) O2, H2SO4, K3PO4 |
| Б) CO2 | 2) CuCl2 (p-p), CuO, KMnO4 (p-p) |
| В) NH3 | 3) CaO, K2CO3, HCl |
| Г) ZnO | 4) BaCl2, SO2 (p-p), Pb(NO3)2 |
| 5) C, KOH, Na2[Zn(OH)4] (p-p) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами в этой реакции: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) Zn и NaOH (p-p) | 1) цинкат натрия и водород |
| Б) Zn и NaOH (расплав) | 2) тетрагидроксоцинкат натрия и водород |
| В) Zn и H2O (нагревание) | 3) оксид цинка и водород |
| Г) Zn и H2SO4 (разб.) | 4) гидроксид цинка и вода |
| 5) сульфат цинка и водород | |
| 6) сульфат цинка, сероводород и вода |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана следующая схема превращений:
![]() Определите, какие из указанных веществ являются веществами Х и Y.
Определите, какие из указанных веществ являются веществами Х и Y.
1) Fe(OH)3
2) CO
3) FeCl3
4) Fe3O4
5) Cl2
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) амилопектин | 1) углеводороды |
| Б) целлюлоза | 2) моносахариды |
| В) мальтоза | 3) дисахариды |
| 4) полисахариды |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня соединений выберите два соединения, которые изомерны гексанолу-2.
1) этиловый эфир бутановой кислоты
2) диизопропиловый эфир
3) изобутанол
4) бутилэтиловый эфир
5) 2-метилбутанол-1
- Из предложенного перечня выберите два вещества, которые не реагируют с водородом.
1) пропан
2) циклопропан
3) дивинил
4) неопентан
5) аллен
- Из предложенного перечня выберите два вещества, которые реагируют с этиленгликолем.
1) Br2 (H2O)
2) KOH
3) HNO3 (разб.)
4) Cu(OH)2
5) Al
- Из предложенного перечня выберите два вещества, которые реагируют с метанолом, но не реагируют с метиламином.
1) O2
2) K
3) C2H5OH
4) HNO2
5) HBr
- Установите соответствие между названием углеводорода и названием алкана, при дегидроциклизации которого образуется этот углеводород: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ УГЛЕВОДОРОДА | НАЗВАНИЕ АЛКАНА |
| А) циклопентан | 1) 2-метилгептан |
| Б) толуол | 2) 2-метилпентан |
| В) 1,3-диметилциклопентан | 3) пентан |
| Г) бензол | 4) 2-метилгексан |
| 5) 2,4-диметилпентан | |
| 6) гексан |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ при нагревании: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | УГЛЕРОДСОДЕРЖАЩИЙ ПРОДУКТ РЕАКЦИИ |
| А) этанол и оксид меди (II) | 1) этаналь |
| Б) этанол и оксид марганца (IV) | 2) ацетат меди (II) |
| В) этанол и уксусная кислота | 3) этилацетат |
| Г) уксусная кислота и оксид меди (II) | 4) ацетат марганца (II) |
| 5) углекислый газ | |
| 6) уксусная кислота |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана схема превращений веществ:
C3H6 → X → C3H4 → Y → CH3 – CH(OH) – CH3
Определите, какие из указанных веществ являются веществами Х и Y.
1) 1,2-дихлорпропан
2) пропаналь
3) 2-бромпропан
4) пропанол-1
5) ацетон
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня выберите гетерогенные реакции.
1) этерификация метанола муравьиной кислотой
2) гидрирование жиров
3) сплавление серы с железом
4) хлорирование метана
5) нейтрализация гидроксида меди (II) азотной кислотой
Запишите номера выбранных ответов.
- Из предложенного перечня выберите внешние воздействия, которые уменьшают скорость реакции растворения мрамора в разбавленной соляной кислоте.
1) понижение общего давления
2) разбавление реакционной смеси
3) добавление раствора гидроксида натрия
4) повышение температуры
5) добавление небольшого количества твёрдого хлорида кальция
Запишите номера выбранных ответов.
- Установите соответствие между уравнением реакции и свойством атома галогена с более низкой электроотрицательностью: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | СВОЙСТВО АТОМА ГАЛОГЕНА С БОЛЕЕ НИЗКОЙ ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬЮ |
| А) I2 + 5Cl2 + 6H2O = 10HCl + 2HIO3 | 1) является окислителем |
| Б) I2 + 2KBrO3 = 2KIO3 + Br2 | 2) является восстановителем |
| В) I2 + 2HClO4 = 2HIO4 + Cl2 | 3) является и окислителем, и восстановителем |
| 4) не изменяет степень окисления |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием вещества и способом его получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | СПОСОБ ПОЛУЧЕНИЯ |
| 1) натрий | 1) только электролиз водного раствора соли |
| 2) магний | 2) только электролиз расплава соли |
| 3) серебро | 3) только электролиз расплава оксида с криолитом |
| 4) алюминий | 4) и электролиз водного раствора соли, и электролиз расплава соли |
| 5) только электролиз водного раствора основания | |
| 6) и электролиз расплава оксида с криолитом, и электролиз расплава соли |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием соли и характером среды её водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЩВАНИЕ СОЛИ | ХАРАКТЕР СРЕДЫ |
| А) тетрагидроксоцинкат калия | 1) кислотная |
| Б) хлорид хрома (II) | 2) щелочная |
| В) сульфид цезия | 3) нейтральная |
| Г) нитрат аммония |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при уменьшении давления в системе: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) Br2 (ж) + H2 (г) ↔ 2HBr (г) | 1) смещается в сторону прямой реакции |
| Б) H2 (г) + Se (к)↔ H2Se (г) | 2) смещается в сторону обратной реакции |
| В) SO2 (г) + Cl2 (г) ↔ SO2Cl2 (ж) | 3) практически не смещается |
| Г) NH3 (г) + HCl (г)↔ NH4Cl (тв) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между реагентами и реактивом, с помощью которого можно их различить (все электролиты находятся в виде разбавленных водных растворов): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГЕНТЫ | РЕАКТИВ |
| А) MgBr2 и (CH3COO)2Mg | 1) KCl |
| Б) K2SO3 и MgSO4 | 2) AgNO3 |
| В) Al и Mg | 3) ZnO |
| Г) HBr и CH3COOH | 4) KOH |
| 5) KNO3 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между веществом и областью его применения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВЕЩЕСТВО | ОБЛАСТЬ ПРИМЕНЕНИЯ |
| А) уголь | 1) дезинфекция воды и отбеливание тканей |
| Б) карборунд | 2) сварка и резка металлов |
| В) гипохлорит натрия | 3) топливо |
| 4) консервант | |
| 5) абразивный материал |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответом к заданиям 27–29 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Затем перенесите это число в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Единицы измерения физических величин в бланке ответа указывать не нужно.
При проведении расчётов для всех элементов кроме хлора используйте значения относительных атомных масс, выраженных целыми числами (Ar(Cl) =35,5).
- К 220 г раствора NaOH с массовой долей щёлочи 10% добавили 23 г натрия. Найдите массовую долю (%) щёлочи в полученном растворе. (Запишите число с точность до сотых.)
- Разложение нитрата меди (II) происходит в соответствии с термохимическим уравнением
2Cu(NO3)2 (тв) = 2CuO (тв) + 4NO2 (г) + O2 (г) — 244 кДж.
Рассчитайте количество энергии (в кДж), затраченное для получения 11,2 л газовой смеси кислорода и оксида азота (IV) (н.у.) по данной реакции. (Запишите число с точностью до десятых.)
- Какую массу (в граммах) оксида хрома (VI) можно растворить в 5,6 г гидроксида калия?(Запишите число с точностью до целых.)
Часть 2
Для записи ответов на задания 30–35 используйте БЛАНК ОТВЕТОВ № 2. Запишите сначала номер задания (30, 31 и т.д.), а затем его подробное решение. Ответы записывайте чётко и разборчиво.
Для выполнения заданий 30, 31 используйте следующий перечень веществ соляная кислота, гидроксид калия, азотная кислота, платина, оксид цинка, фосфорная кислота: Допустимо использование водных растворов веществ.
- Из предложенного перечня выберите вещества, в результате окислительно-восстановительной реакции между которыми выделяется бесцветный газ. Причём одна структурная единица восстановителя отдаёт 4 электрона, а окислителя – принимает 3 электрона. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
- Из предложенного перечня выберите два вещества, которые вступают в реакцию ионного обмена, которое описывается кратким ионным уравнением с суммой коэффициентов равной 8. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
- Смешали растворы сульфата меди (II) и карбоната натрия. Выпавший осадок выделили, высушили и прокалили. Затем полученный твёрдый остаток смешали с нашатырём и снова прокалили. В результате чего образовалось два простых и два сложных вещества. Образовавшееся твёрдое простое вещество растворили в растворе хлорида железа (III). Напишите уравнения четырёх описанных реакций.
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
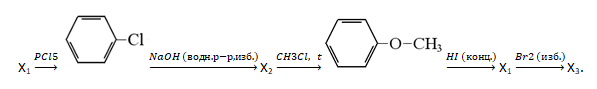 При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
- В два последовательно соединённых электролизёра поместили по 100 г растворов: в первый 10% (по массе) раствор хлорида натрия, во второй – 20% (по массе) хлорида золота (III) и включили ток. Через некоторое время электролиз прекратили и масса раствора в первом электролизёре уменьшилась на 3,285 г. Определите массовую долю хлорида золота (III) во втором электролизёре после электролиза. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
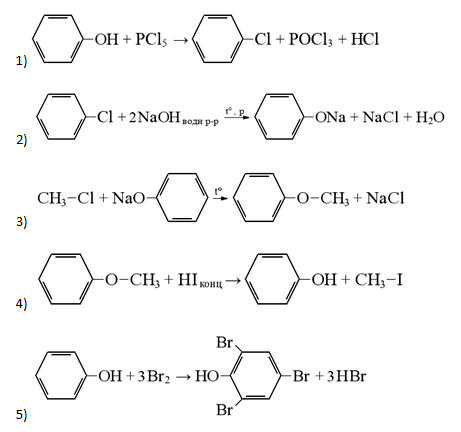
- Вещество А содержит 65,06% углерода, 6,02% водорода, 28,92% кислорода по массе. Известно, что вещество А окисляется до бензойной кислоты. Также известно, что вещество А при взаимодействии с бромоводородом даёт бромопроизводное Б. При воздействии на это бромопроизводное Б спиртового раствора щёлочи происходит дегидрогалогенирование и образуется соль ненасыщенной кислоты.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
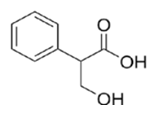
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
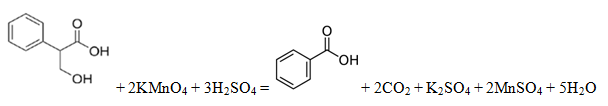
3) напишите уравнение реакции окисления вещества А перманганатом калия в присутствии серной кислоты (используйте структурные формулы органических веществ).
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Ответы:
Первая часть:
- 23
- 451
- 14
- 14
- 331
- 45
- 34
- 4523
- 2135
- 24
- 443
- 24
- 14
- 34
- 23
- 3456
- 1132
- 15
- 235
- 23
- 222
- 2246
- 2121
- 1322
- 2442
- 351
- 25,62
- 24,4
- 5
Вторая часть:
- 3Pt + 4HNO3 + 12HCl = 3PtCl4 + 4NO↑ + 8H2O
Pt0 – 4e = Pt+4 3
N+5 + 3e = N+2 4
Азот в степени окисления +5 (или HNO3) является окислителем.
Платина в степени окисления 0 (или Pt) является восстановителем.
- 3KOH + H3PO4 = K3PO4 + 3H2O
3K+ + 3OH— + H3PO4 = 3K+ + PO43- + 3H2O
3OH— + H3PO4 = PO43- + 3H2O
- 1) 2CuSO4 + 2Na2CO3 + H2O = (CuOH)2CO3↓ + 2Na2SO4 + CO2↑
2) (CuOH)2CO3 = 2CuO + CO2↑ + H2O (прокаливание)
3) 3CuO + 2NH4Cl = 3Cu + 3H2O↑ + 2HCl↑ + N2↑ (прокаливание)
4) Cu + 2FeCl3 = 2FeCl2 + CuCl2
- 12%
Видео-объяснение смотрите на Ютуб по ссылке или ниже
35. 1. Общая формула вещества А – CxHyOz
x : y : z = 65,06/12 : 6,02/1 : 28,92/16 = 5,422 : 6,02 : 1,808 = 3 : 3,33 : 1 = 9 : 10 : 3. Следовательно, молекулярная формула С9Н10О3.
- Соединение С9Н10О3 окисляется до бензойной кислоты, значит его основу составляет бензолное кольцо. Отсюда следует, что заместитель имеет три атома углерода. Так как в конце всех превращений (описанных в задаче) образуется соль ненасыщенной кислоты, то вещество А содержит карбоксильную группу. Из трёх атомов кислорода в веществе А два входят в состав карбоксила, а третий принадлежит спиртовому гидроксилу, так как вещество А при взаимодействии с бромоводородом образует бромпроизводное Б, что невозможно в случае наличия фенольного гидроксила. При взаимодействии на это бромпроизводное спиртового раствора щёлочи происходит дегидрогалогенирование и образуется соль ненасыщенной карбоновой кислоты, следовательно, спиртовой гидроксил находится в β-положении по отношению к карбоксильной группе, так как именно β-гидроксикислоты при нагревании отщепляют воду и образуют ненасыщенные соединения.
3. Уравнение реакции:
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ всех лет (реальные, пробные и тренировочные задания) вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку

В 9 задании под 2) тетрагидроксоцинкат натрия и водород, а не тетрагидроксоцинкат калия
Спасиюо за внимательность! Поправил.