Оксид серы (VI) — SO3 (серный ангидрид)
Физические свойства
Бесцветная летучая маслянистая жидкость, t°пл. = 17°C; t°кип. = 66°С; на воздухе «дымит», сильно поглощает влагу (хранят в запаянных сосудах).
SO3 + H2O → H2SO4
SO3 хорошо растворяется в 100%-ной серной кислоте, этот раствор называется олеумом.
Получение
1) 2SO2 + O2 → 2SO3 (катализатор – V2O5, при 450˚С)
2) Fe2(SO4)3 → Fe2O3 + 3SO3 (разложение при нагревании)
Химические свойства
1) Серный ангидрид — кислотный оксид.
Взаимодействие с водой
При растворении в воде дает сильную двухосновную серную кислоту:
SO3 + H2O → H2SO4
Диссоциация протекает ступенчато:
H2SO4→ H+ + HSO4— (первая ступень, образуется гидросульфат – ион)
HSO4— → H+ + SO42- (вторая ступень, образуется сульфат – ион)
H2SO4 образует два ряда солей — средние (сульфаты) и кислые (гидросульфаты)
Взаимодействие со щелочами
2NaOH + SO3 → Na2SO4 + H2O
NaOH + SO3 (избыток) → NaHSO4
Взаимодействие с основными оксидами
Na2O + SO3 → Na2SO4
2) SO3 — сильный окислитель.
Серная кислота
Физические свойства серной кислоты:
Тяжелая маслянистая жидкость (“купоросное масло”);
плотность 1,84 г/см3; нелетучая, хорошо растворима в воде – с сильным нагревом; t°пл. = 10,3°C, t°кип. = 296°С, очень гигроскопична, обладает водоотнимающими свойствами (обугливание бумаги, дерева, сахара).
Теплота гидратации настолько велика, что смесь может вскипать, разбрызгиваться и вызывать ожоги. Поэтому необходимо добавлять кислоту к воде, а не наоборот, поскольку при добавлении воды к кислоте более легкая вода окажется на поверхности кислоты, где и сосредоточится вся выделяющаяся теплота.
Промышленное производство серной кислоты (контактный способ):
1) 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
2) 2SO2 + O2 V2O5→ 2SO3
3) nSO3 + H2SO4 → H2SO4·nSO3 (олеум)
Измельчённый очищенный влажный пирит (серный колчедан) сверху засыпают в печь для обжига в “кипящем слое“. Снизу (принцип противотока) пропускают воздух, обогащённый кислородом.
Из печи выходит печной газ, состав которого: SO2, O2, пары воды (пирит был влажный) и мельчайшие частицы огарка (оксида железа). Газ очищают от примесей твёрдых частиц (в циклоне и электрофильтре) и паров воды (в сушильной башне).
В контактном аппарате происходит окисление сернистого газа с использованием катализатора V2O5 ( пятиокись ванадия) для увеличения скорости реакции. Процесс окисления одного оксида в другой является обратимым. Поэтому подбирают оптимальные условия протекания прямой реакции – повышенное давление (т.к прямая реакция идет с уменьшением общего объема) и температура не выше 500 С ( т.к реакция экзотермическая).
В поглотительной башне происходит поглощение оксида серы (VI) концентрированной серной кислотой.
Поглощение водой не используют, т.к оксид серы растворяется в воде с выделением большого количества теплоты, поэтому образующаяся серная кислота закипает и превращается в пар. Для того, чтобы не образовывалось сернокислотного тумана, используют 98%-ную концентрированную серную кислоту. Оксид серы очень хорошо растворяется в такой кислоте, образуя олеум: H2SO4·nSO3
Химические свойства серной кислоты:
H2SO4 – сильная двухосновная кислота, одна из самых сильных минеральных кислот, из-за высокой полярности связь Н – О легко разрывается.
1) В водном растворе серная кислота диссоциирует, образуя ион водорода и кислотный остаток:
H2SO4 = H+ + HSO4–;
HSO4– = H+ + SO42-.
Суммарное уравнение:
H2SO4 = 2H+ + SO42-.
2) Взаимодействие серной кислоты с металлами:
Разбавленная серная кислота растворяет только металлы, стоящие в ряду напряжений левее водорода:
Zn0 + H2+1SO4(разб) → Zn+2SO4 + H2
3) Взаимодействие серной кислоты с основными оксидами:
CuO + H2SO4 → CuSO4 + H2O
4) Взаимодействие серной кислоты с гидроксидами:
H2SO4 + 2NaOH → Na2SO4 + 2H2O
H2SO4 + Cu(OH)2 → CuSO4 + 2H2O
5) Обменные реакции с солями:
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Образование белого осадка BaSO4 (нерастворимого в кислотах) используется для обнаружения серной кислоты и растворимых сульфатов (качественная реакция на сульфат ион).
Особые свойства концентрированной H2SO4 :
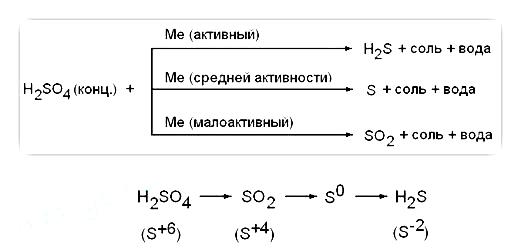
1) Концентрированная серная кислота является сильным окислителем; при взаимодействии с металлами (кроме Au, Pt) восстанавливаться до S+4O2, S0 или H2S-2 в зависимости от активности металла. Без нагревания не реагирует с Fe, Al, Cr – пассивация. При взаимодействии с металлами, обладающими переменной валентностью, последние окисляются до более высоких степеней окисления, чем в случае с разбавленным раствором кислоты: Fe0 → Fe3+, Cr0 → Cr3+, Mn0 → Mn4+,Sn0 → Sn4+
Активный металл
8 Al + 15 H2SO4(конц.)→4Al2(SO4)3 + 12H2O + 3H2S
4│2Al0 – 6e– → 2Al3+ – окисление
3│ S6+ + 8e → S2– восстановление
4Mg+ 5H2SO4 → 4MgSO4 + H2S + 4H2O
Металл средней активности
2Cr + 4 H2SO4(конц.)→ Cr2(SO4)3 + 4 H2O + S
1│ 2Cr0 – 6e →2Cr3+– окисление
1│ S6+ + 6e → S0 – восстановление
Металл малоактивный
2Bi + 6H2SO4(конц.)→ Bi2(SO4)3 + 6H2O + 3SO2
1│ 2Bi0 – 6e → 2Bi3+ – окисление
3│ S6+ + 2e →S4+ – восстановление
2Ag + 2H2SO4 →Ag2SO4 + SO2 + 2H2O
2) Концентрированная серная кислота окисляет некоторые неметаллы как правило до максимальной степени окисления, сама восстанавливается до S+4O2:
С + 2H2SO4(конц) → CO2 + 2SO2 + 2H2O
S+ 2H2SO4(конц) → 3SO2 + 2H2O
2P+ 5H2SO4(конц)→5SO2 + 2H3PO4 + 2H2O
3) Окисление сложных веществ:
Серная кислота окисляет HI и НВг до свободных галогенов:
2 КВr + 2Н2SO4 = К2SО4 + SO2 + Вr2 + 2Н2О
2 КI + 2Н2SО4 = К2SO4 + SO2 + I2 + 2Н2О
Концентрированная серная кислота не может окислить хлорид-ионы до свободного хлора, что дает возможность получать НСl по реакции обмена:
NаСl + Н2SO4(конц.) = NаНSO4 + НСl
Серная кислота отнимает химически связанную воду от органических соединений, содержащих гидроксильные группы. Дегидратация этилового спирта в присутствии концентрированной серной кислоты приводит к получению этилена:
С2Н5ОН = С2Н4 + Н2О.
Обугливание сахара, целлюлозы, крахмала и др. углеводов при контакте с серной кислотой объясняется также их обезвоживанием:
C6H12O6 + 12H2SO4 = 18H2O + 12SO2↑ + 6CO2↑.