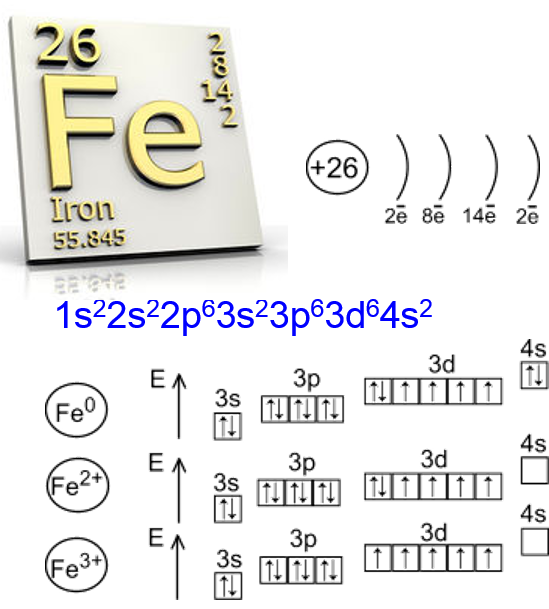
Элемент железо входит в побочную подгруппу VIII группы периодической системы и относится к d-элементам.
Железо известно очень давно. Это самый распространенный в земной коре металл (около 4 % по массе) и самый распространенный в природе переходный металл. В природе железо существует только в виде соединений. Чистое железо имеет преимущественно внеземное происхождение.
Железо используются в виде сплавов: чугуна, стали и ковкого железа. Эти сплавы различаются различным содержанием углерода, в чугуне более 1,7 %, в стали – от 0,3 % до 1,7 %, а в ковком железе – менее 0,3 %. В состав так называемых легированных сталей входят хром, вольфрам, молибден, никель, ванадий, титан, кобальт и другие металлы, что дает возможность получать стали с разными полезными свойствами.
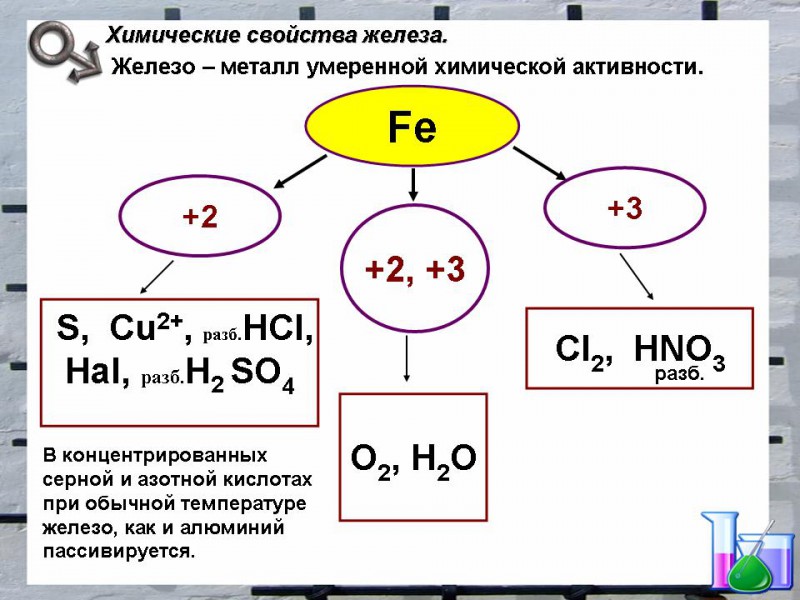
Чистое железо – блестящий серебристо-белый металл. В ряду активности стоит до водорода и растворяется в соляной и разбавленной серной кислотах, выделяя водород. При действии концентрированной серной и азотной кислот железо пассивируется – покрывается тонкой защитной пленкой оксида, поэтому эти кислоты перевозят в железных цистернах.
В соединениях железо проявляет различные степени окисления, в основном +2 и +3, известны также высшие степени окисления железа +4, +5 и +6. Железо является металлом средней активности. При нагревании выше 200 °С в отсутствие паров воды железо покрывается плотной пленкой оксида. Этот процесс называется воронением.
Железо взаимодействует с парами воды при нагревании:
3Fe + 4H2O = Fe3O4 + 4H2
С галогенами железо образует соответствующие соли железа (II и III), а при избытке галогена образуется галогенид железа (III):
2Fe + 3Cl2 = 2FeCl3
Железо растворяется в разбавленных соляной и серной кислотах с образованием солей железа (II):
Fe + 2HCl = FeCl2 + H2
Разбавленная азотная кислота растворяет железо с выделением оксидов азота и нитрата железа (III).
Во влажном воздухе и воде железо разрушается – коррозирует, образуя ржавчину. Коррозия – это окислительно-восстановительный процесс, при котором металл окисляется. Наиболее интенсивно он идет при одновременном присутствии воды и кислорода. В сухом воздухе или в воде, не содержащей кислорода, железо не ржавеет. Суммарное уравнение реакции ржавления железа можно записать так:
4Fe + 6H2O + 3O2 = 4Fe(OH)3
В настоящее с коррозией борются нанесением защитных покрытий, легированием, применением ингибиторов.
Получение:
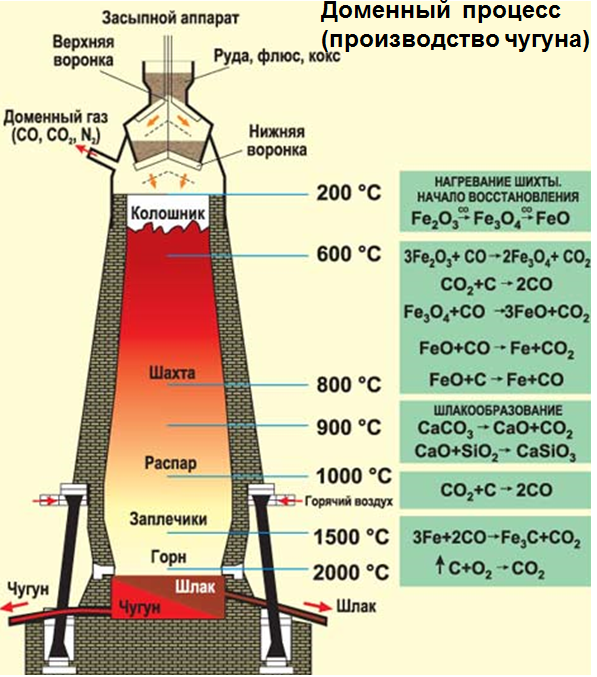
Доменный процесс (производство чугуна):
C + O2 = CO2, CO2 + C ↔ 2CO
3Fe2O3 + CO = 2(Fe2Fe32)O4+ CO2
(Fe2Fe32)O4+ CO= 3FeO + CO2
FeO + CO= Fe + CO2
(чугун содержит до 6,67% углерода в виде зерен графита и цементита Fe3C);
Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева. Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов. При этом оксиды либо улавливаются в виде отходящих газов (CO2, SO2), либо связываются в легко отделяемый шлак – смесь Ca3(PO4)2 и CaSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Оксид железа(II) FеО. Основный оксид. Черный, имеет ионное строение Fе2+ O2-. При нагревании вначале разлагается, затем образуется вновь. Не образуется при сгорании железа на воздухе. Не реагирует с водой. Разлагается кислотами, сплавляется со щелочами. Медленно окисляется во влажном воздухе. Восстанавливается водородом, коксом. Участвует в доменном процессе выплавки чугуна. Применяется как компонент керамики и минеральных красок. Уравнения важнейших реакций:
FеО + 2НС1 (разб.) = FеС12 + Н2O
FеО + 4НNO3 (конц.) = Fе(NO3)3 +NO2↑ + 2Н2O
FеО + Н2 =Н2O + Fе (особо чистое) (350°С)
FеО + С(кокс) = Fе + СО (выше 1000 °С)
FеО + СО = Fе + СO2 (900°С)
4FеО + 2Н2O(влага) + O2 (воздух) →4FеО(ОН) (t)
6FеО + O2 = 2Fe3O4 (300—500°С)
Получение в лаборатории: термическое разложение соединений железа (II) без доступа воздуха:
Fе(ОН)2 = FеО + Н2O (150-200 °С)
FеСОз = FеО + СO2 (490-550 °С)
Оксид железа (III) – Fe3 O4 . Двойной оксид. Черный, имеет ионное строение Fe2+(Fе3+)2(O2-)4. Термически устойчив до высоких температур. Не реагирует с водой. Разлагается кислотами. Восстанавливается водородом, раскаленным железом. Участвует в доменном процессе производства чугуна. Применяется как компонент минеральных красок (железный сурик), керамики, цветного цемента. Продукт специального окисления поверхности стальных изделий (чернение, воронение). По составу отвечает коричневой ржавчине и темной окалине на железе. Применение брутто-формулы Fe3O4 не рекомендуется. Уравнения важнейших реакций:
2Fe3O4 = 6FеО + O2 (выше 1538 °С)
Fe3O4 + 8НС1 (разб.) = FеС12 + 2FеС13 + 4Н2O
Fe3O4 +10НNO3 (конц.) =3Fе(NO3)3 + NO2↑+ 5Н2O
Fe3O4 + O2 (воздух) = 6Fе2O3 (450-600°С)
Fe3O4 + 4Н2 = 4Н2O + 3Fе (особо чистое, 1000 °С)
Fe3O4 + СО =ЗFеО + СO2 (500—800°C)
Fe3O4 + Fе ⇌4FеО (900—1000 °С , 560—700 °С)
Получение: 3Fe + 2O2 (воздух) = Fe3O4
В природе – оксидная руда железа магнетит.
Оксид железа(III) Fе2О3. Амфотерный оксид с преобладанием основных свойств. Красно-коричневый, имеет ионное строение (Fе 3+)2(O2-)3. Термически устойчив до высоких температур. Не образуется при сгорании железа на воздухе. Не реагирует с водой, из раствора выпадает бурый аморфный гидрат Fе2O3 nН2О. Медленно реагирует с кислотами и щелочами. Восстанавливается монооксидом углерода, расплавленным железом. Сплавляется с оксидами других металлов и образует двойные оксиды – шпинели (технические продукты называются ферритами). Применяется как сырье при выплавке чугуна в доменном процессе, катализатор в производстве аммиака, компонент керамики, цветных цементов и минеральных красок, при термитной сварке стальных конструкций, как носитель звука и изображения на магнитных лентах, как полирующее средство для стали и стекла.
Уравнения важнейших реакций:
6Fе2O3 = Fe3O4 +O2 (1200—1300 °С)
Fе2O3 + 6НС1 (разб.) →2FеС13 + ЗН2O (t) (600°С,р)
Fе2O3 + 2NaОН (конц.) →Н2O+ 2NаFеO2 (красн.) диоксоферрат(III)
Fе2О3 + МО= Fe3O4 (М=Сu, Мn, Fе, Ni, Zn)
Fе2O3 + ЗН2 =ЗН2O+ 2Fе (особо чистое, 1050—1100 °С)
Fе2O3 + Fе = ЗFеО (900 °С)
3Fе2O3 + СО = 2Fe3O4 + СO2 (400—600 °С)
Получение в лаборатории – термическое разложение солей железа (III) на воздухе:
Fе2(SO4)3 = Fе2O3 + 3SO3 (500-700 °С)
4{Fе(NO3)3 9 Н2O} = 2Fе2O3 + 12NO2+ 3O2 + 36Н2O (600-700 °С)
В природе – оксидные руды железа гематит Fе2O3 и лимонит Fе2O3 nН2O
Гидроксид железа (II) Fе(ОН)2. Основный гидроксид. Белый (иногда с зеленоватым оттенком), связи Fе – ОН преимущественно ковалентные. Термически неустойчив. Легко окисляется на воздухе, особенно во влажном состоянии (темнеет). Нерастворим в воде. Реагирует с разбавленными кислотами, концентрированными щелочами. Типичный восстановитель. Промежуточный продукт при ржавлении железа. Применяется в изготовлении активной массы железоникелевых аккумуляторов.
Уравнения важнейших реакций:
Fе(OН)2 = FеО + Н2O (150-200 °С, в атм.N2)
Fе(ОН)2 + 2НС1 (разб.) =FеС12 + 2Н2O
Fе(ОН)2 + 2NаОН (> 50%) = Nа2[Fе(ОН)4] ↓(сине-зеленый) (кипячение)
4Fе(ОН)2 (суспензия) + O2 (воздух) →4FеО(ОН)↓ + 2Н2O (t)
2Fе(ОН)2 (суспензия) +Н2O2 (разб.) = 2FеО(ОН)↓ + 2Н2O
Fе(ОН)2 + КNO3 (конц.) = FеО(ОН)↓ + NO↑+ КОН (60 °С)
Получение: осаждение из раствора щелочами или гидратом аммиака в инертной атмосфере:
Fе2+ + 2OH (разб.) = Fе(ОН)2↓
Fе2+ + 2(NH3Н2O) = Fе(ОН)2↓+ 2NH4