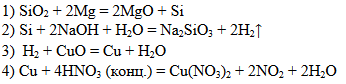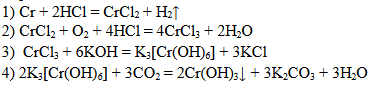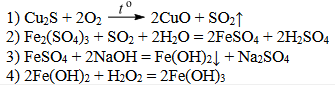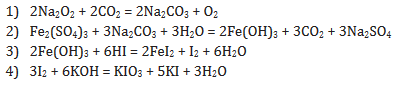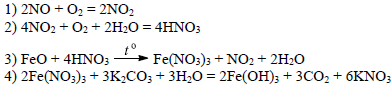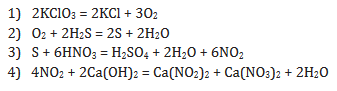Взаимосвязь различных классов неорганических веществ. Часть 3
Предлагаем вам сборку заданий по теме Взаимосвязь различных классов неорганических веществ. Ответы вы найдёте внизу страницы.
ВНИМАНИЕ — в ЕГЭ 2022 года это будет задание 31
Задание 14
Оксид алюминия сплавили с карбонатом калия. Полученный продукт растворили в избытке серной кислоты. К образовавшемуся раствору добавили избыток аммиачной воды. Выпавший осадок отделили и обработали избытком раствора гидроксида натрия.
Напишите уравнения четырёх описанных реакций.
Задание 15
Питьевую соду обработали избытком соляной кислоты. Выделившийся газ пропустили над раскалённым углём. В результате чего образовался новый газ, который затем смешали с сернистым газом при нагревании. Затем твёрдый продукт реакции полностью растворили в концентрированном растворе гидроксида натрия. Напишите уравнения четырёх описанных реакций.
Задание 16
Задание 17
Задание 18
Через раствор силиката калия пропустили избыток углекислого газа. Выпавший осадок отделили и прокалили, а затем сплавили с фосфатом кальция и углём. Полученное простое вещество растворили на холоду в концентрированной азотной кислоте, причём выделился бесцветный газ. Напишите уравнения четырёх описанных реакций.
Задание 19
Оксид алюминия растворили в водном растворе гидроксида натрия. К получившемуся раствору добавили избыток раствора азотной кислоты. Затем добавили избыток раствора сульфида калия2. Образовавшийся осадок выделили и прокалили. Напишите уравнения четырёх описанных реакций.
Задание 20
К раствору хлорида хрома (III) добавили избыток раствора едкого кали. К образовавшемуся раствору добавили бром. После завершения реакции к раствору прилили раствор серной кислоты. Образовавшуюся при этом соль хрома выделили, растворили в воде и полученный раствор прилили к раствору хлорида бария, в результате чего образовался жёлтый осадок. Напишите уравнения четырёх описанных реакций.
Задание 21
Смесь порошков гидросульфата натрия и металлического магния подвергли совместному сплавлению, в результате чего наблюдали образование газа с неприятным запахом. Выделившийся газ собрали в колбу и смешали с сернистым газом и нагревали в течении некоторого времени. В результате в колбе наблюдали образование жёлтого дыма. Через некоторое время все твёрдые частицы дыма осели на дно колбы, а колбу заполнили «веселящим газом» (содержит атомы азота в своём составе) и снова нагрели. По окончанию реакции твёрдых веществ в колбе не осталось. А затем избыток одного из получившихся газов пропустили через раствор карбоната натрия. Напишите уравнения четырёх описанных реакций.
Задание 22
Смешали растворы сульфата меди (II) и карбоната натрия. Выпавший осадок выделили, высушили и прокалили. Затем полученный твёрдый остаток смешали с нашатырём и снова прокалили. В результате чего образовалось два простых и два сложных вещества. Образовавшееся твёрдое простое вещество растворили в растворе хлорида железа (III). Напишите уравнения четырёх описанных реакций.
Ответы:
Задание 14
Задание 15
NaHCO3 + HCl = NaCl + H2O + CO2
CO2 + C = 2CO
CO + SO2 = 2CO2 + S
3S + +6NaOH = Na2SO3 + 2Na2S + 3H2O
или 4S + 6NaOH = Na2S2O3 + 2Na2S + 3H2O
Задание 16
Al4C3 + 6O2 = 2Al2O3 + 3CO2
Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
4Mg + 5H2SO4 (конц.) = 4MgSO4 + H2S↑ + 4H2O
2Na[Al(OH)4] + H2S = 2Al(OH)3↓ + Na2S + 2H2O
Задание 17
2Na + 2H2O = 2NaOH + H2
4H2 + Fe3O4 3Fe + 4H2O
2Fe + 6H2SO4 (конц.) Fe2(SO4)3 + 3SO2 + 6H2O
Fe2(SO4)3 + 3K2CO3 + 3H2O = 3K2SO4 + 2Fe(OH)3 + 3CO2
Задание 18
1) K2SiO3 + 2CO2 + 2H2O = H2SiO3↓ + 2KHCO3
2) H2SiO3 = SiO2 + H2O
3) Ca3(PO4)2 + 3SiO2 + 5C = 3CaSiO3 + 2P + 5CO
4) 3P + 5HNO3 + 2H2O = 3H3PO4 + 5NO
Задание 19
1) Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
2) Na[Al(OH)4] + 4HNO3 = NaNO3 + Al(NO3)3 + 4H2O
3) 2Al(NO3)3 + 3K2S + 6H2O = 3H2S↑ + 2Al(OH)3↑ + 6KNO3
4) 2Al(OH)3 = Al2O3 + 3H2O (при нагревании)
Задание 20
1) CrCl3 + 4KOH = K[Cr(OH)4] + 3KCl
или CrCl3 + 6KOH = K3[Cr(OH)6] + 3KCl
2) 2K[Cr(OH)4] + 3Br2 + 8KOH = 2K2CrO4 + 6KBr + 8H2O
или 2 K3[Cr(OH)6] + 3Br2 + 4KOH = 2K2CrO4 + 6KBr + 8H2O
3) 2K2CrO4 + 2H2SO4 = K2Cr2O7 + 2KHSO4 + H2O (допустимо образование K2SO4)
4) K2Cr2O7 + 2BaCl2 + H2O = 2BaCrO4↓ + 2KCl + 2HCl
Задание 21
1) 10NaHSO4 + 4Mg = 4MgSO4 + 5Na2SO4 + H2S↑ + 4H2O (сплавление)
2) 2H2S + SO2 = 3S↓ + 2H2O (нагревание)
3) S + 2N2O = SO2 + 2N2 (нагревание)
4) Na2CO3 + 2SO2 + H2O = 2NaHSO3 + CO2↑
Задание 22
1) 2CuSO4 + 2Na2CO3 + H2O = (CuOH)2CO3↓ + 2Na2SO4 + CO2↑
2) (CuOH)2CO3 = 2CuO + CO2↑ + H2O (прокаливание)
3) 3CuO + 2NH4Cl = 3Cu + 3H2O↑ + 2HCl↑ + N2↑ (прокаливание)
4) Cu + 2FeCl3 = 2FeCl2 + CuCl2
Также предлагаем вам плейлист видео-уроков и видео-объяснений заданий на эту тему:
Также:
- Посмотреть реальные, досрочные и пробные варианты ЕГЭ всех лет вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки для подготовки к ЕГЭ вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ вы можете здесь, нажав на эту строку
- Все видео-объяснения вы можете найти на YouTube канале, нажав на эту строку