Предлагаем вашему вниманию второй пробный вариант для подготовки к ЦТ по химии 2021: ответы представлены в конце страницы.
Скачать РТ 2020/2021 вариант 2 в виде pdf-файла
ВНИМАНИЕ: все задания составлены автором самостоятельно и не являются копией заданий ЦТ и РТ. Если вам необходимы оригинальные задания, то вам надо записываться на этапы РТ (на сайте РИКЗ) и покупать сборники реальных заданий ЦТ и РТ в книжных магазинах.
Вариант 2
Для получения полного доступа к сайту переходите по ссылке: http://www.yoursystemeducation.com/poluchit-video/. В полном доступе вы найдёте условия и видео-объяснения заданий-аналогов из всех этапов РТ начиная с 2014 года, а также всех заданий-аналогов ЦТ начиная с самого первого ЦТ 2004 года.
Вариант содержит 50 заданий и состоит из части А (38 заданий) и части В (12 заданий). На выполнение всего теста отводится 150 минут. Необходимые справочные материалы – «Периодическая система химических элементов Д.И. Менделеева», «Растворимость кислот, оснований и солей в воде», Электрохимический ряд активности металлов» — приведены в конце теста.
При расчётах принять молярный объём газа (Vm) 22,4 дм3/моль. Значения относительных атомных масс химических элементов (кроме хлора, для которого Ar = 35,5) следует округлять до целого числа. При решении заданий можно пользоваться микрокалькулятором.
Часть А
Для получения приближённого значения чисел в промежуточных расчётах округлите их до третьего знака после запятой по правилам округления. Конечный результат округлите, ориентируясь на числа, предложенные в ответе.
В каждом задании только ОДИН из предложенных вариантов ответа является верным.
А1. Укажите элемент, который находится в одном периоде с иодом:
1) сурьма
2) селен
3) хлор
4) марганец
5) свинец
А2. Укажите семейство элементов, к которому относится элемент, содержащий в атоме 34 электрона:
1) s-семейство
2) p-семейство
3) d-семейство
4) семейство щелочных металлов
5) семейство благородных газов
А3. Укажите возможную массу (г) атома цезия:
1) 220,78∙10-27
2) 55
3) 220,78∙10-24
4) 133
5) 78
А4. В ряду элементов Be, B, C согласно положению в периодической системе химических элементов:
1) увеличивается размер атомов
2) уменьшается число электронных оболочек в атомах
3) сначала увеличивается, а затем уменьшается число протонов в ядрах атомов
4) увеличивается число неспаренных электронов в атомах в основном состоянии
5) уменьшается электроотрицательность
А5. Укажите порцию простого вещества, в котором содержится белый фосфор Р4 химическим количеством 4 моль (н.у.):
1) 31 г
2) 89,6 дм3
3) 124 г
4) 60 г
5) 24,08∙1023
А6. Выберите правильное утверждение относительно химических связей в молекуле воды:
1) имеется двойная связь
2) энергии всех связей одинаковы
3) одна связь образована по донорно-акцепторному механизму
4) образованы р-электронами водорода и кислорода
5) являются водородными
А7. Укажите пары веществ, в которых совпадают валентности серы:
1) SO2 и Na2SO4
2) H2S и FeS2
3) SCl2 и SO3
4) H2SO3 и SO3
5) CuS и SO2
А8. Укажите ряд, в котором оба оксида реагируют с разбавленной азотной кислотой:
1) CaO и SeO3
2) CuO и CO2
3) Cs2O и ZnO
4) SO3 и SO2
5) NO2 и NO
А9. Щёлочь образуется в результате реакции между веществами:
1) SO3 и H2O
2) Fe2O3 и H2O
3) NaOH и CuSO4
4) Zn и RbOH
5) SrO и H2O
А10. Укажите формулу вещества, при добавлении к которому водного раствора метилоранжа приводит к изменению окраски индикатора на красную:
1) FeO
2) NaCl
3) HBr
4) K2O
5) Na2[Zn(OH)4]
А11. В водном растворе с гидрокарбонатом рубидия при стандартных условиях реагируют вещества, формулы которых:
а) CO2, б) BaCO3, в) Ba(OH)2, г) NaOH:
1) а, в
2) а, г
3) б, в
4) а, б
5) в, г
А12. Укажите ряд элементов, которые могут существовать в виде нескольких простых веществ:
1) H, S, Na
2) O, C, Cl
3) B, He, S
4) C, P, O
5) K, Ne, F
А13. Укажите вещества, с которыми может реагировать водород:
а) хлор, б) азот, в) этан, г) фосфор, д) селен, е) неон:
1) в, г, е
2) а, б, г
3) в, г, д
4) а, б, д
5) б, в, г
А14. Хлор выступает только в роли окислителя в химической реакции, протекающей по схеме:
1) AgNO3 + NaCl → AgCl + NaNO3
2) HCl + Zn → ZnCl2 + H2
3) ZnCl2 + F2 → ZnF2 + Cl2
4) H2 + Cl2 → HCl
5) KClO3 → KCl + KClO4
А15. Серная кислота любой концентрации реагирует с веществами:
а) гидроксидом меди (II), б) хлоридом натрия (тв.),
в) гидрокарбонатом калия, г) серебром:
1) а, б
2) б, г
3) а, в
4) в, г
5) б, в
А16. Аммиак пропустили через раствор азотной кислоты, в результате чего образовалось вещество А, к которому, затем, добавили концентрированный раствор гидроксида калия при нагревании, в результате чего образовалось вещество Б. Азотсодержащим веществом Б является:
1) оксид азота (II)
2) аммиак
3) нитрат аммония
4) нитрид калия
5) оксид азота (IV)
А17. Укажите название вещества, водный раствор которого не может долго храниться в закрытой стеклянной колбе:
1) нитрат натрия
2) гидроксид лития
3) сульфат калия
4) пропановая кислота
5) ацетат рубидия
А18. Укажите процесс, в котором металл подвергается восстановлению:
1) взаимодействие оксида меди (II) с водородом при нагревании
2) разложение нитрата цинка
3) разложение гидроксида алюминия
4) разложение водой гидрида калия
5) взаимодействие железа с кислородом при нагревании
А19. Массовая доля металл в соединении состава МеОН равна 88,67%. Укажите справедливые утверждения относительно этого металла:
а) является активным металлом,
б) расположен в IВ-группе,
в) входит в состав медного купороса,
г) реагирует с водой:
1) а, б
2) а, г
3) б, в
4) в, г
5) б, г
А20. Укажите пары веществ, с которыми реагирует при 25С гидроксид алюминия:
1) гидроксид калия и бромоводородная кислота
2) муравьиная кислота и сульфат цинка
3) гидроксид лития и гидроксид железа (II)
4) нитрат калия и оксид серы (IV)
5) сера и фосфор
А21. Для уменьшения скорости химической реакции Zn (тв.) + 2H+ = Zn2+ + H2 (г.) + Q необходимо:
1) увеличить концентрацию ионов водорода
2) повысить температуру
3) увеличить давление
4) увеличить концентрацию ионов цинка
5) уменьшить концентрацию ионов водорода
А22. Выберите ответ, в котором понижение давления сместит равновесие системы в сторону исходных веществ:
1) 2CO2 (г) ↔ 2CO (г) + O2 (г)
2) FeO (тв) + CO (г) ↔ Fe (тв) + CO2 (г)
3) H2 (г) + Br2 (г) ↔ 2HBr (г)
4) 2SO2 (г) + O2 (г) ↔ 2SO3 (г)
5) 2NH3 (г) ↔ 3H2 (г) + N2 (г)
А23. Имеется разбавленный водный раствор азотистой кислоты. Степень диссоциации HNO2 уменьшится при добавлении к нему:
а) меди,
б) воды,
в) иодоводорода,
г) оксида азота (IV):
1) а, б
2) а, в
3) б, в
4) в, г
5) б, г
А24. В водном растворе в значительных количествах одновременно НЕ могут присутствовать ионы, которые образуются при диссоциации веществ пары:
1) AlCl3 и KOH
2) ZnCl2 и H2SO4
3) Fe(NO3)3 и HBr
4) MgSO4 и HCl
5) NaOH и Ba(OH)2
А25. Имеются водные растворы с одинаковыми молярными концентрациями растворённых веществ. Установите соответствие между формулой растворённого вещества и рН раствора (сильные электролиты диссоциируют полностью):
| Вещество | рН |
| А) HCl
Б) CH3COOH В) CsOH Г) NH3 |
1) 13,9
2) 11,0 3) 4,3 4) 1,7 |
1) А2Б4В3Г1
2) А4Б2В1Г3
3) А3Б4В2Г1
4) А4Б3В1Г2
5) А2Б4В1Г3
А26. Коэффициент перед формулой продукта восстановления в уравнении химической реакции, схема которой KCrO2 + Cl2 + KOH → K2CrO4 + KCl + H2O, равен:
1) 2
2) 3
3) 6
4) 8
5) 10
А27. Укажите молекулярную формулу насыщенного альдегида:
1) С5Н8О
2) С5Н6О
3) С5Н10О
4) С5Н12О
5) С5Н10О2
А28. Укажите название вещества, которого НЕ существует:
1) 4-бром-2-метилпентен-1
2) 2-бром-2-метилпентен-2
3) 1-бром-2-метилпентен-1
4) 1-бром-2-метилпентен-2
5) 2-бром-3-метилпентен-1
А29. Число структурных изомеров относящихся к одному классу органических веществ у 2,3-диметилбутана равно:
1) 3
2) 4
3) 5
4) 6
5) 2
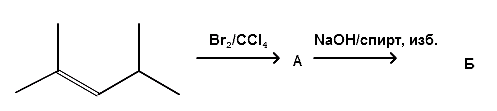
А30. Укажите класс органических веществ, к которому относится вещество Б, согласно превращению:
1) алкадиен
2) двухатомный спирт
3) алкен
4) алкин
5) альдегид
А31. Этанол реагирует с веществами:
а) натрием, б) гидроксидом натрия, в) бромидом калия,
г) муравьиной кислотой, д) оксидом меди (II), е) кислородом:
1) а, г, д, е
2) б, в, г, е
3) а, б, г, д
4) а, в, г, д
5) б, в, г, д
А32. Укажите верное утверждение для вещества с молекулярной формулой C6H5OH:
1) нетоксичное вещество, получают из каменноугольной смолы
2) кристаллическое вещество (н.у.), реагирует со щелочами
3) малорастворимо в воде при 20 С, используется для получения нитроглицерина
4) проявляет слабые основные свойства, качественной реакцией на раствор этого вещества – является реакция с бромом
5) имеет тривиальное название бензол, реагирует с калием
А33. Этин в лаборатории можно получить в результате:
1) добавления спиртового раствора щёлочи к хлорэтану
2) добавлением воды к ацетилену в присутствии солей ртути
3) гидролиз карбида кальция
4) нагревания этанола в присутствии концентрированной серной кислоты при температуре выше 170 С
5) гидрированием этена
А34. Гидроксид натрия реагирует с каждым веществом пары:
1) метанол и метановая кислота
2) этиловый спирт и фенол
3) пропанол-1 и этиловый эфир уксусной кислоты
4) этановая кислота и фенол
5) триолеин и пропанол-2
А35. Выберите на картинке формулу вещества, которое вступает в реакцию этерификации:
2) 2
3) 3
4) 4
5) ни одно из веществ
А36. В отличие от глюкозы сахароза:
1) имеет формулу C6H12O6
2) не является альдегидоспиртом
3) плохо растворяется в воде
4) относится к гексозам
5) НЕ горит в кислороде
А37. Укажите возможное число дипептидов, которые могут образоваться из смеси цистеина и серина:
1) 1
2) 2
3) 3
4) 4
5) 5
А38. Образец этилена имеет среднюю молярную массу 100800 г/моль. Укажите число структурных звеньев в этой макромолекуле этилена:
1) 4200
2) 7800
3) 3600
4) 8400
5) 12600
Часть В
При решении задач в промежуточных расчётах для получения приближенного значения чисел округлите их до третьего знака после запятой по правилам округления, а конечный результат – до целого числа. Единицы измерения числовых величин не указывайте.
Ответы, полученные при выполнении заданий, запишите в бланк ответов. Каждую букву, цифру пишите в отдельной клеточке (начиная с первой) по образцам, указанным в бланке.
В1. Белое очень гигроскопичное вещество А растворяется в воде с образованием раствора слабой кислоты Б, которая реагирует с гидроксидом В, образуя соль Г. Прокаливая соль Г с коксом и песком, получают простое вещество Д (состоящее из четырёхатомных молекул), атомы которого входят в состав вещества А.
Определите все зашифрованные вещества и в ответе укажите соответствие между буквой вещества и его молярной массой (г/моль), например: А4Б4В3Г1Д2.
| Вещество | Молярная масса |
| А | 1) 74 |
| Б | 2) 98 |
| В | 3) 124 |
| Г | 4) 142 |
| Д | 5) 310 |
В2. Выберите верные утверждения о пероксиде водорода:
- При нагревании в присутствии оксида марганца (IV) разлагается на простые вещества.
- В химических реакциях может как окисляться, так и восстанавливаться.
- Валентность атома кислорода в молекуле равна I.
- Между молекулами образуются водородные связи.
- Молекулярная и простейшая формулы НЕ совпадают.
- При н.у. – газообразное вещество.
В3. При сжигании аминокислоты (CxHyOzNk) массой 26,7 г в избытке кислорода образуется углекислый газ массой 39,9 г, вода массой 18,9 г и азот объёмом (н.у.) 3,36 л. Укажите суммарное число всех атомов в одной молекуле аминокислоты.
В4. Метиламин объёмом 2 дм3 смешали с кислородом объёмом 6 дм3 при нормальных условиях и подожгли. Определите плотность (г/дм3) образовавшейся газовой смеси после приведения её к нормальным условиям.
В5. Определите сумму молярных масс (г/моль) органических веществ молекулярного строения Б, Г и Д, которые зашифрованны буквами.
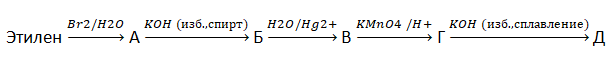 В6. Для получения веществ по указанной схеме превращений
В6. Для получения веществ по указанной схеме превращений
Hg → Hg(NO3)2 → Hg(OH)2 → HgSO4 → Hg
Выберите реактивы из предложенных:
1 – Na2SO4; 2 – NaOH; 3 – Ni; 4 – H2SO4; 5 – KNO3; 6 – AgNO3.
Ответ запишите цифрами в порядке следования превращений, например: 1324
В7. В четырёх пронумерованных пробирках находятся водные растворы неорганических веществ, содержащие ионы Be2+, NH4+, SO42-, SO32-.
Об этих растворах известно:
— при приливании в пробирки №1 и №4 раствора гидроксида калия в пробирке №1 происходит выделение газа (н.у.) с характерным запахом, а в пробирке №4 сначала выпадает осадок, который затем растворяется в избытке щёлочи;
— при добавлении к содержимому пробирок №2 и №3 соляной кислоты в пробирке №2 выделяется газ (н.у.), а в пробирке №3 ничего не происходит. Установите соответствие между ионом и номером пробирки, в которой находится вещество, содержащее указанный ион.
Ионы: А) Be2+, Б) NH4+, В) SO42-, Г) SO32-.
№ пробирки: 1, 2, 3, 4
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность, например, А2Б3В4Г1.
В8. Укажите утверждения, которые верно характеризуют амилозу:
- Является составной частью целлюлозы.
- Макромолекулы имеют линейное (неразветвлённое) строение.
- Состоит из остатков α-глюкозы в линейной (нециклической) форме.
- В воде растворима лучше, чем амилопектин.
- Остатки глюкозы связаны химической связью – О – между первым атомом одной молекулы глюкозы и четвёртым атомом другой молекулы глюкозы.
- НЕ подвергается гидролизу.
В9. Определите степень диссоциации (%) муравьиной кислоты в её 0,46%-ном (по массе) водном растворе (плотность раствора принять за 1 г/см3), если суммарная концентрация всех частиц, образованных муравьиной кислотой (молекул и ионов) в растворе равна 0,11 моль/л.
В10. Рассчитайте массовую долю силиката натрия в растворе, полученным при растворении в 57 см3 40%-ного раствора гидроксида натрия с плотностью 1404 кг/м3 всего кремния, образовавшегося в результате длительного нагревания (все реакции пройдут до конца) магния массой 28,8 г с оксидом кремния (IV) массой 24 г.
В11. Образец минерала массой 105,6 г, в котором массовая доля меди 0,8, массовая доля серы 0,2, сожгли в избытке кислорода. В результате реакции выделилось 320 кДж теплоты. Рассчитайте тепловой эффект (кДж) сгорания минерала химическим количеством 1 моль.
В12. Один и тот же сосуд поочерёдно заполняли при одинаковых условиях тремя различными газами, причём масса заполненного сосуда (с учётом массы сосуда) каждый раз составляла 832, 942 и 858 г соответственно. Определите молярную массу (г/моль) первого газа, если известно, что плотность второго газа по третьему равна 2,45, а плотность третьего газа по водороду – 14,5.
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Ответы:
Часть А
- 1
- 2
- 3
- 4
- 5
- 2
- 2
- 3
- 5
- 3
- 5
- 4
- 4
- 4
- 3
- 2
- 2
- 1
- 2
- 1
- 5
- 4
- 4
- 1
- 4
- 3
- 3
- 2
- 2
- 1
- 1
- 2
- 3
- 4
- 1
- 2
- 4
- 3
Часть В
- А4Б2В1Г5Д3
- 245
- 13
- 2
- 102
- 6243
- А4Б1В3Г2
- 245
- 10
- 29
- 485
- 16
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Материалы этого варианта РТ (тесты, задания, задачи, видео) разработаны автором самостоятельно и не являются копией каких-либо других заданий, в том числе заданий, разработанных РИКЗом (Республиканским институтом контроля знаний). При составлении заданий использованы идеи, которые были использованы составителями ЦТ и РТ, что не является нарушением авторского права. Все материалы используются исключительно в образовательных целях.
В доказание вышесказанного, привожу выдержки из Закона Республики Беларусь «Об авторском праве и смежных правах»:
Статья 7. Произведения, не являющиеся объектами авторского права
Пункт 2. Авторское право не распространяется на собственно идеи, методы, процессы, системы, способы, концепции, принципы, открытия, факты, даже если они выражены, отображены, объяснены или воплощены в произведении.
Статья 32. Свободное использование объектов авторского права и смежных прав
Пункт 2. Допускается воспроизведение отрывков из правомерно обнародованных произведений (цитирование) в оригинале и переводе в исследовательских, образовательных, полемических, критических или информационных целях в том объеме, который оправдан целью цитирования.
Статья 36. Свободное использование произведений в образовательных и исследовательских целях
Пункт 2. Статьи и иные малообъемные произведения, правомерно опубликованные в сборниках, а также газетах, журналах и других печатных средствах массовой информации, отрывки из правомерно опубликованных литературных и иных произведений могут быть воспроизведены посредством репродуцирования и иного воспроизведения в образовательных и исследовательских целях.
Посмотреть видео-объяснения каждого задания ЦТ, РТ и ДРТ всех лет вы можете получив полный доступ к сайту кликнув здесь «Получить все материалы сайта»
- Посмотреть все пробные варианты ЦТ 2021 вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Больше заданий РТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЦТ вы можете найти здесь, нажав на эту строку