Скачать Пробный вариант 4. ЕГЭ 2021 по химии с ответами в формате pdf
Часть 1
Ответом к заданиям 1–26 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Цифры в ответах на задания 5, 8, 9, 11, 16, 17, 21–26 могут повторяться.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду
1) Ba 2) F 3) Ga 4) S 5) K
- Из предложенного перечня выберите два элемента, которые содержат одинаковое число спаренных электронов на внешнем энергетическом уровне в основном состоянии.
Запишите в поле ответа номера выбранных элементов.
- Выберите три элемента, принадлежащих к большим периодам Периодической системы, и расположите их в порядке возрастания атомного радиуса.
Запишите в поле ответа номера выбранных элементов в нужной последовательности.
- Из предложенного перечня химических элементов выберите два таких, которые способны проявлять отрицательные степени окисления в сложных веществах.
Запишите в поле ответа номера выбранных элементов.
- Из предложенного перечня выберите два вещества с наибольшей длиной связи между атомами внутри молекулы.
1) иод
2) бромоводород
3) кислород
4) фтороводород
5) иодид калия
Запишите в поле ответа номера выбранных веществ.
- Усоответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) негашеная известь | 1) соль |
| Б) халькопирит | 2) кислота |
| В) поташ | 3) оксид |
| 4) основание |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня металлов выберите два таких, которые реагируют как с концентрированной серной, так и с концентрированной азотной кислотами при комнатной температуре.
1) Cu
2) Fe
3) Al
4) Zn
5) Cr
Запишите в поле ответа номера выбранных веществ.
- Даны две пробирки с раствором бромоводородной кислоты. В одну из пробирок добавили нерастворимое в воде вещество Х, которое является неэлектролитом. В результате добавленное вещество полностью растворилось, , а выделения газа при этом не происходило. Во вторую пробирку добавили раствор соли Y. В этом случае наблюдали выделение газа. Из предложенного перечня выберите вещества Х и Y, которые могут вступить в описанные реакции.
1) CaCO3
2) Na2S
3) BaO
4) BeO
5) Zn
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) ацетат серебра | 1) NaOH, HBr, HF |
| Б) серная кислота (конц.) | 2) HCl (разб.), NaBr, CsI |
| В) гидроксид цинка | 3) HCl (конц.), CuS, (CH3COO)2Zn |
| Г) оксид меди (I) | 4) Hg, HgO, HgS |
| 5) H2SO4, CO, Al |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) Cl2 + KOH (холодный р-р) | 1) KCl + H2O |
| Б) Cl2 + KOH (горячий р-р) | 2) KClO + H2O |
| В) ClO2 + KOH | 3) KClO3 + H2O |
| Г) HClO3 + KOH | 4) KCl + KClO + H2O |
| 5) KCl + KClO3 + H2O | |
| 6) KClO2 + KClO3 + H2O |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана следующая схема превращений:
 Определите, какие из указанных веществ являются веществами Х и Y.
Определите, какие из указанных веществ являются веществами Х и Y.
1) PH3
2) K2HPO4
3) K2O
4) P4
5) K
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) олеодистеарин | 1) амины |
| Б) анилин | 2) аминокислоты |
| В) орто-крезол | 3) арены |
| 4) сложные эфиры | |
| 5) пептиды |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня выберите два вещества, в молекулах которых нет третичных атомов углерода.
1) метилциклогексан
2) стирол
3) 2,2,3-триметилбутан
4) бутен-2
5) этаналь
- Из предложенного перечня выберите два вещества, с каждым из которых может взаимодействовать пропилен.
1) гидроксид диамминсеребра (I)
2) гидроксид калия (спиртовой раствор)
3) раствор брома в тетрахлорметане
4) бензол (в присутствии фосфорной кислоты)
5) гидроксид меди (II)
- Из предложенного перечня выберите два вещества, которые реагируют со всеми веществами ряда – метанол, фенол, уксусная кислота.
1) KOH (p-p)
2) K
3) Ag2O (NH3 p-p)
4) Cu(OH)2
5) O2
- Из предложенного перечня выберите два вещества, с которыми не реагирует аминобензол.
1) бромоводородная кислота
2) метанол
3) гидроксид натрия (водн. р-р)
4) ацетилхлорид
5) бромная вода
- Установите соответствие между химической реакцией и названием органического вещества, преимущественно образующимся в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАКЦИЯ | НАЗВАНИЕ ПРОДУКТА |
| А) крекинг гексана | 1) пропан |
| Б) дегидрирование пропена | 2) пропин |
| В) гидратация бутена-1 | 3) неопентан |
| Г) изомеризация 2-метилбутана | 4) бутанол-1 |
| 5) бутанон-2 | |
| 6) бутанол-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между реагирующими веществами и продуктами их взаимодействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
 Запишите в таблицу выбранные цифры под соответствующими буквами.
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана схема превращений веществ:
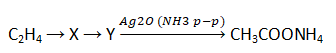 Определите, какие из указанных веществ являются веществами Х и Y.
Определите, какие из указанных веществ являются веществами Х и Y.
1) С2H6
2) CH4
3) C2H2
4) CH3CHO
5) CH3COOH
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня выберите схемы, которые соответствуют реакции замещения.
1) C2H6 + Br2 →
2) Al + O2 →
3) Cs2O + HCl →
4) KBr + Cl2 →
5) CaCO3 + SiO2 →
Запишите номера выбранных ответов.
- Из предложенного перечня внешних воздействий выберите воздействия, которые не влияют на скорость реакции, уравнение которой:
Fe (тв) + 2HCl (р-р) = FeCl2 (р-р) + H2 (г).
1) изменение температуры
2) измельчение железа
3) изменение давления
4) изменение концентрации кислоты
5) изменение концентрации хлорида железа (II)
Запишите номера выбранных ответов.
- Установите соответствие между схемой реакции и свойством, которое проявляет атом азота в ней: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | СВОЙСТВО АЗОТА |
| А) K + NH3 → KNH2 + H2 | 1) является окислителем |
| Б) CH3NH2 + HNO3 → [CH3NH3]NO3 | 2) является восстановителем |
| В) N2H4 + Zn + HCl → NH4Cl + ZnCl2 | 3) является и окислителем, и восстановителем |
| 4) не является окислителем или восстановителем |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием вещества и продуктами, которые выделяются на инертном аноде при электролизе его водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | ПРОДУКТ НА АНОДЕ |
| 1) серная кислота | 1) водород |
| 2) бромид калия | 2) фтор |
| 3) фторид серебра (I) | 3) бром |
| 4) пропионат калия | 4) кислород |
| 5) этан, углекислый газ | |
| 6) бутан, оксид углерода (IV) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой соли и цветом, в который окрашивает метилоранж её водный раствор: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
| А) CsNO3 | 1) красный |
| Б) ZnSO4 | 2) жёлтый |
| В) NaHS | 3) оранжевый |
| Г) K3PO4 | 4) малиновый |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между воздействием и направлением, в которое сместит это воздействие равновесие обратимой реакции
C3H7OH (г) ↔ C3H6 (г) + H2O (г) – Q: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВНЕШНЕЕ ВОЗДЕЙСТВИЕ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) нагревание реакционного сосуда | 1) смещается вправо |
| Б) внесение никелевого катализатора | 2) смещается влево |
| В) выведение спирта из реакционного сосуда | 3) практически не смещается |
| Г) уменьшение объёма сосуда |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулами двух веществ (находятся в виде разбавленных водных растворов) и реагентом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛЫ ВЕЩЕСТВ | РЕАГЕНТ |
| А) AlCl3 и CuCl2 | 1) AgNO3 |
| Б) NaF и HNO3 | 2) NaOH |
| В) NaBr и NaF | 3) H2SO4 |
| Г) KBr и HBr | 4) KBr |
| 5) Na2CO3 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между аппаратом, используемым при промышленном получении серной кислоты, и его предназначением: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| АППАРАТ | ПРЕДНАЗНАЧЕНИЕ |
| А) циклон | 1) осушение от водяных паров |
| Б) печь | 2) очистка от мелких частиц пыли |
| В) электрофильтр | 3) очистка от крупных частиц пыли |
| 4) обжиг пирита | |
| 5) окисление оксида серы (IV) | |
| 6) поглощение серного ангидрида конц. серной кислотой |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответом к заданиям 27–29 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Затем перенесите это число в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Единицы измерения физических величин в бланке ответа указывать не нужно.
При проведении расчётов для всех элементов кроме хлора используйте значения относительных атомных масс, выраженных целыми числами (Ar(Cl) =35,5).
- Какую массу соли (г) надо добавить к 400 г 18%-ного раствора соли для получения раствора с массовой долей растворённого вещества 22%? (Запишите число с точность до тысячных.)
- Графит сгорает в атмосфере кислорода согласно термохимическому уравнению:
C (тв) + O2 (г) = CO2 (г) +393,5 кДж.
Рассчитайте количество энергии в кДж, которое выделится при сгорании графита массой 3 г. (Запишите число с точностью до тысячных.)
- Вычислите объём водорода (л, н.у.), который необходимо взять для получения 34 г аммиака, если выход реакции составляет 100%. (Запишите число с точностью до десятых.)
Часть 2
Для записи ответов на задания 30–35 используйте БЛАНК ОТВЕТОВ № 2. Запишите сначала номер задания (30, 31 и т.д.), а затем его подробное решение. Ответы записывайте чётко и разборчиво.
Для выполнения заданий 30, 31 используйте следующий перечень веществ: иодат калия, гидразин, хлорид алюминия, магний, карбонат натрия, фосфат аммония. Допустимо использование водных растворов веществ.
- Из предложенного перечня выберите вещества, в результате окислительно-восстановительной реакции между которыми одна молекула восстановителя отдаёт 4 электрона, а окислитель восстанавливается до минимальной степени окисления. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
- Из предложенного перечня выберите два вещества, при протекании реакции ионного обмена в водном растворе между которыми выделяется газ и образуется осадок. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
- Смесь порошков гидросульфата натрия и металлического магния подвергли совместному сплавлению, в результате чего наблюдали образование газа с неприятным запахом. Выделившийся газ собрали в колбу и смешали с сернистым газом и нагревали в течении некоторого времени. В результате в колбе наблюдали образование жёлтого дыма. Через некоторое время все твёрдые частицы дыма осели на дно колбы, а колбу заполнили «веселящим газом» (содержит атомы азота в своём составе) и снова нагрели. По окончанию реакции твёрдых веществ в колбе не осталось. А затем избыток одного из получившихся газов пропустили через раствор карбоната натрия. Напишите уравнения четырёх описанных реакций.
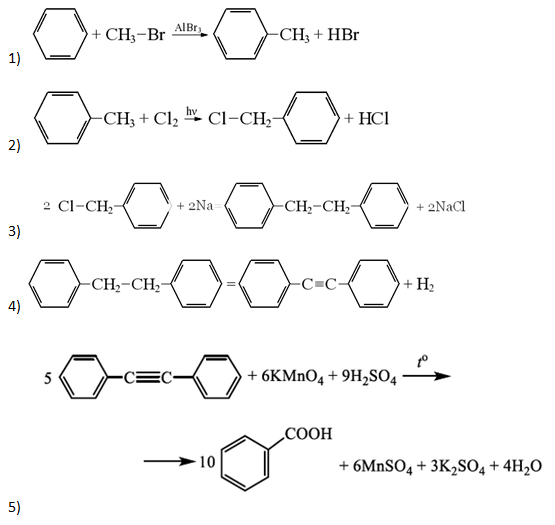
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
 При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
- К 200 г раствора нитрата алюминия с массовой долей соли 12,78% добавили 123,9 мл раствора гидроксида натрия с массовой долей щёлочи 0,12 и плотностью 1,13 г/мл. Полученную смесь упарили и прокалили до постоянной массы. Определите массовую долю кислорода как элемента в твёрдом остатке после прокаливания.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
- При сгораниии 13,7 г органического вещества А получили 15,68 л углекислого газа, 1,12 л азота (н.у.) и 6,3 г воды.
Известно, что вещество А содержит в составе одной молекулы 5 вторичных атомов углерода , один третичный и один первичный атом, а функциональная группа находится в пара-положении. Вещество А при реакции с парами хлороводорода в присутствии железа при нагревании переходит в органическое вещество Б немолекулярного строения.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества;
2) составьте структурную формулу вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А парами хлороводорода в присутствии железа при нагревании (используйте структурные формулы органических веществ).
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Ответы:
Первая часть:
- 13
- 351
- 24
- 12
- 311
- 14
- 42
- 2415
- 4563
- 32
- 413
- 45
- 34
- 25
- 23
- 1263
- 2761
- 34
- 145
- 35
- 441
- 4346
- 3122
- 1322
- 2515
- 342
- 20,513
- 98,375
- 67,2
Вторая часть:
- 3N2H4 + 2KIO3 = 2KI + 3N2↑ + 6H2O
2N-2 – 4e = N20 3
I+5 + 6e = I-1 2
Иод в степени окисления +5 (или KIO3) является окислителем.
Азот в степени окисления -2 (или N2H4) является восстановителем.
- 2AlCl3 + 3Na2CO3 + 3H2O = 6NaCl + 2Al(OH)3↓ + 3CO2↑
2Al3+ + 6Cl— + 6Na+ +3CO32- + 3H2O = 6Na+ + 6Cl— + 2Al(OH)3↓ + 3CO2↑
2Al3+ + 3CO32- + 3H2O = 2Al(OH)3↓ + 3CO2↑
- 1) 10NaHSO4 + 4Mg = 4MgSO4 + 5Na2SO4 + H2S↑ + 4H2O (сплавление)
2) 2H2S + SO2 = 3S↓ + 2H2O (нагревание)
3) S + 2N2O = SO2 + 2N2 (нагревание)
4) Na2CO3 + 2SO2 + H2O = 2NaHSO3 + CO2↑
34. 45,34%.
Видео-объяснение смотрите на Ютуб по ссылке или ниже
- 1) исходное органическое вещество точно содержит в своём составе атомы элементов углерод, азот и водород, так как при сгорании этого вещества образуются углекислый газ, газ азот и вода. А кислород как может входить в состав это вещества, так может и не входить. Проверить это можно сложив массы атомов элементов углерода, азота и водорода, если эта сумма будет равна массе исходного органического вещества, то кислорода нет, а если масса окажется меньше – то кислород есть, и разница между массой вещества за вычетом масс атомов элементов углерода, азота и водорода и есть масса атомов элемента кислорода.
Найдём эти массы:
n = m/M, n = V/Vm
m = n ∙ M,
n (CO2) = 15,68 л / 22,4 л/моль = 0,7 моль
n (С) = n (СО2) = 0,7 моль
m (C) = 0,7 моль ∙ 12 г/моль = 8,4 г
М(Н2О) = 18 г/моль
n (H2O) = 6,3 г / 18 г/моль = 0,35 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 0,35 моль = 0,7 моль
m (H) = 0,7 моль ∙ 1 г/моль = 0,7 г
n (N2) = 1,12 л / 22,4 л/моль = 0,05 моль
n (N) = 2 ∙ n (N2) = 2 ∙ 0,05 моль = 0,1 моль
m (N) = 0,1 моль ∙ 14 г/моль = 1,4 г
m (C) + m (H) + m (N) = 8,4 г + 0,7 г + 1,4 г = 10,5 г, что НЕ равно массе исходного вещества, а значит атомы кислорода присутствуют в веществе.
m (O) = 13,7 г – 10,5 г = 3,2 г
n (O) = 3,2 г / 16 г/моль = 0,2 моль
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (N) : n (O) = 0,7 : 0,7 : 0,1 : 0,2 = 7 : 7 : 1 : 2
Следовательно молекулярная формула вещества: C7H7NO2.
2) Анализируя информацию о веществе А, можно предположить, что это вещество является ароматическим (по указанию первичных, вторичных и третичных атомов углерода). Также для определения класса/группы перебираем известные в школе кислородсодержащие соединения и делаем вывод, что под получившуюся молекулярную формулу подходят либо нитросоединение либо аминокислота. Но так как вещество реагирует с железом и хлороводородом, то узнаём реакцию Зинина, по которой нитрогруппа переходит в аминогруппу с последующей реакцией с кислотой и с образованием органической соли, которая и является веществом Б немолекулярного строения. Вариант с аминокислотой исключаем, так как для реакции аминокислоты с HCl железо не нужно.
2) следовательно, структурная формула: 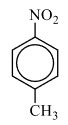 3) уравнение реакции вещества А парами хлороводорода в присутствии железа при нагревании с образованием органической соли Б:
3) уравнение реакции вещества А парами хлороводорода в присутствии железа при нагревании с образованием органической соли Б:
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ всех лет (реальные, пробные и тренировочные задания) вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку


Добрый вечер. Спасибо за вариант. Подскажите ,пожалуйста,почему в 7 второй ответ 2,а не 1? И там,и там газ. Как ученик должен выбирать ответ?
Здравствуйте. Спасибо за вопрос. Дело в том, что в задании указано, что добавили РАСТВОР соли Y — вещество 1 (CaCO3) не растворимо в воде, а значит раствора НЕ образует, а вот вещество 2 (Na2S) — это растворимая соль, поэтому это правильный ответ.
Здравствуйте,почему в 1 задание ответ ответ 13 у бария же на внешнем 2 спаренных 6s2, а у галлия нет спаренных электронов 4p1
Здравствуйте. Внешний слой у галлия — это не только 4р1, но 4s2, поэтому на внешнем слое галлия содержится 2 спаренных электрона (4s2) и один неспаренный электрон (4р1). А убария, как вы и сказали, тоже 2 спаренных электрона (6s2).
Здравствуйте! Подходит ли в 18 задании ответ 54? Ведь из этилена можно получить этанол, потом окислить его до этаналя и уже потом при взаимодействии с аммиачным раствором оксида серебра получить ацетат амония?
Здравствуйте. Подходит и ваш вариант. Спасибо за внимательность! Я устраню это несоответствие, поменяю пятый ответ этанол на уксусную кислоту.
здравствуйте, почему в 14 задании не подходит ответ 15?
Здравствуйте. Потому что в ответе 1 есть метанол — это спирт, а спирты со щелочами (КОН) НЕ реагируют