В природе металлы существуют как в свободном, так и в связанном виде. В свободном виде существуют малоактивные металлы: платина, золото, серебро. Но в основном металлы встречаются в виде различных соединений. Многие металлы способны реагировать друг с другом. Продукты взаимодействия металлов между собой называются сплавами.
Атомы металлов имеют небольшое число валентных электронов. Они слабо связаны с ядром и могут легко отрываться от него. В результате в узлах кристаллической решетки появляются положительно заряженные ионы, а между ними свободно перемещаются электроны – образуется так называемый «электронный газ». Вид связи между положительными ионами, осуществляемой за счет притяжения электронов, свободно перемещающихся по кристаллу, называется металлической.
Металлы имеют многие специфические свойства. Все они, за исключением ртути, при обычных условиях твердые вещества с характерным блеском, хорошо проводят электрический ток и тепло. Большинство металлов может коваться, тянуться и прокатываться. Электро- и теплопроводность металла объясняются наличием в нем свободных электронов.
Металлы делятся на легкие и тяжелые, отличаются друг от друга по твердости: самые мягкие – щелочные, их можно резать ножом; самый твердый – хром. Металлы делятся на легкоплавкие и тугоплавкие. В металлургии металлы делят на черные (железо, марганец, хром) и цветные (все остальные металлы).
Металлы всегда выступают в роли восстановителей. Способность отдавать электроны проявляется у металлов в разной степени. Чем легче металл отдает электроны, тем он активнее и тем более энергично взаимодействует с неметаллами и ионами других металлов. По активности все металлы располагаются в определенной последовательности, образуя электрохимический ряд напряжений.
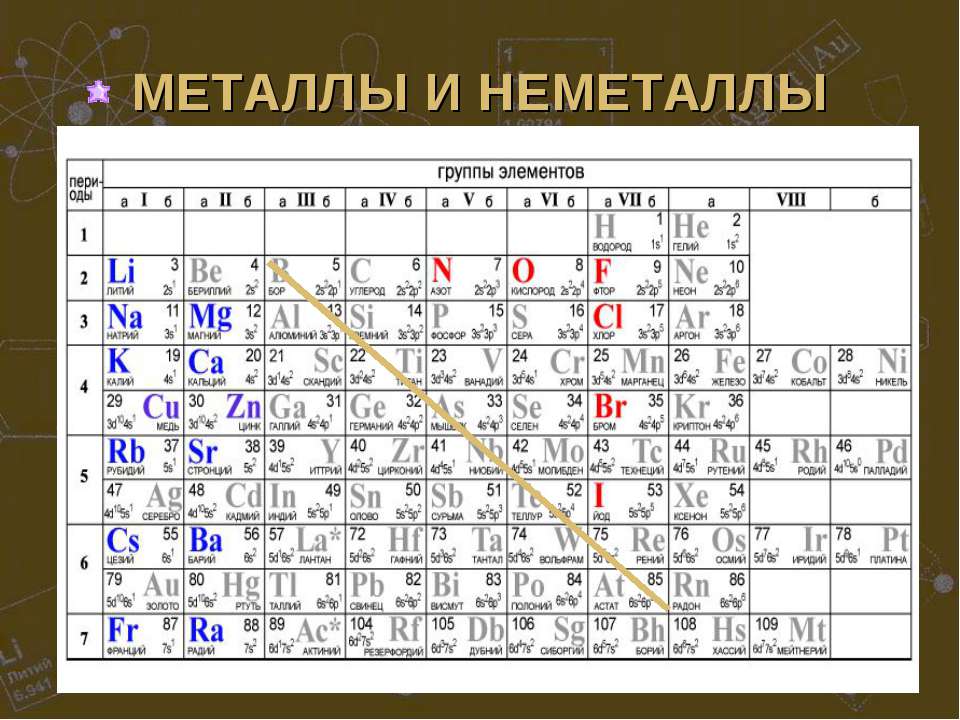
Наиболее типичные металлы расположены в начале периодов (начиная со второго), далее слева направо металлические свойства ослабевают. В группе сверху вниз металлические свойства усиливаются, т.к увеличивается радиус атомов (за счет увеличения числа энергетических уровней). Это приводит к уменьшению электроотрицательности (способности притягивать электроны) элементов и усилению восстановительных свойств (способность отдавать электроны другим атомам в химических реакциях).
Типичными металлами являются s-элементы (элементы IА-группы от Li до Fr. элементы ПА-группы от Мg до Rа). Общая электронная формула их атомов ns1-2. Для них характерны степени окисления + I и +II соответственно.
Небольшое число электронов (1-2) на внешнем энергетическом уровне атомов типичных металлов предполагает легкую потерю этих электронов и проявление сильных восстановительных свойств, что отражают низкие значения электроотрицательности. Отсюда вытекает ограниченность химических свойств и способов получения типичных металлов.
Характерной особенностью типичных металлов является стремление их атомов образовывать катионы и ионные химические связи с атомами неметаллов. Соединения типичных металлов с неметаллами – это ионные кристаллы «катион металлаанион неметалла», например К+ Вг–, Сa2+ О2-. Катионы типичных металлов входят также в состав соединений со сложными анионами – гидроксидов и солей, например Мg2+(OН–)2, (Li+)2СO32-.
Металлы А-групп, образующие диагональ амфотерности в Периодической системе Ве-Аl-Gе-Sb-Ро, а также примыкающие к ним металлы (Gа, In, Тl, Sn, Рb, Вi) не проявляют типично металлических свойств. Общая электронная формула их атомов ns2np0-4 предполагает большее разнообразие степеней окисления, большую способность удерживать собственные электроны, постепенное понижение их восстановительной способности и появление окислительной способности, особенно в высоких степенях окисления (характерные примеры – соединения Тl III, РbIV, Вiv). Подобное химическое поведение характерно и для большинства (d-элементов, т. е. элементов Б-групп Периодической системы (типичные примеры – амфотерные элементы Сr и Zn).
Это проявление двойственности (амфотерности) свойств, одновременно металлических (основных) и неметаллических, обусловлено характером химической связи. В твердом состоянии соединения нетипичных металлов с неметаллами содержат преимущественно ковалентные связи (но менее прочные, чем связи между неметаллами). В растворе эти связи легко разрываются, а соединения диссоциируют на ионы (полностью или частично). Например, металл галлий состоит из молекул Ga2, в твердом состоянии хлориды алюминия и ртути (II) АlСl3 и НgСl2 содержат сильно ковалентные связи, но в растворе АlСl3 диссоциирует почти полностью, а НgСl2 – в очень малой степени (да и то на ионы НgСl+ и Сl–).